
NGUỒN GỐC CỦA CFDNA LÀ GÌ?
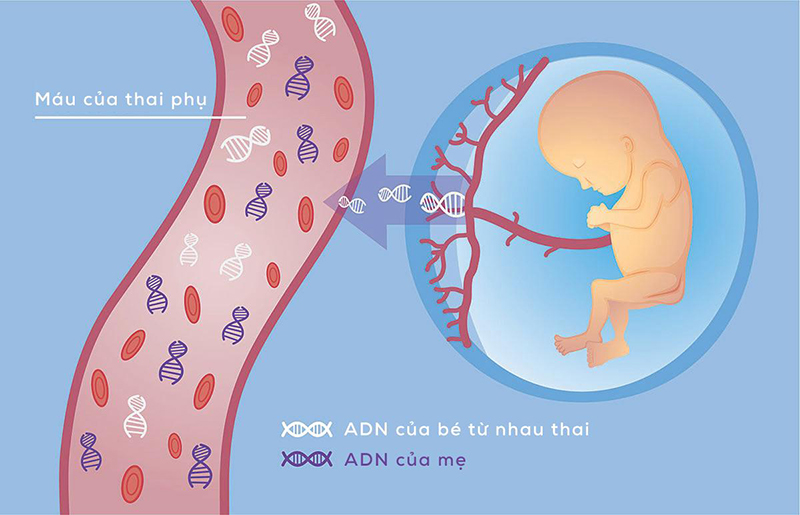
ADN tự do của thai nhi (cell free fetal DNA - cffDNA) lưu hành trong máu mẹ được phát hiện lần đầu bởi Lo và cộng sự vào năm 1997 [2]. Việc phát hiện cfDNA trong huyết tương thai phụ được coi là bước tiến đột phá và là nguồn mẫu lý tưởng được ứng dụng trong sàng lọc trước sinh không xâm lấn.
Các nghiên cứu chỉ ra rằng DNA thai tự do có nguồn gốc từ rau thai [3] và có thể phát hiện sớm từ tuần thai thứ 5 của thai kì [4]. cffDNA là các phân mảnh DNA ngắn, 80,0% có chiều dài < 200 bp, tương đương đoạn DNA ngắn được giải phóng từ quá trình chết theo chương trình của tế bào [5] và Nồng độ cfDNA dao động rất lớn trong quá trình mang thai, tăng theo tuổi thai [6] và bị ảnh hưởng của rất nhiều yếu tố khác nhau.
Ứng dụng phân tích cfDNA dựa trên công nghệ giải trình tự gen thế hệ mới (NGS) bắt đầu từ năm 2011 [7] và cho đến thời điểm hiện tại thì xét nghiệm NIPT đã được ứng dụng rộng rãi trong thực hành lâm sàng. Xét nghiệm NIPT với độ chính xác cao có ưu thế vượt trội hơn hẳn so với các phương pháp sàng lọc trước sinh truyền thống khác và giúp giảm đáng kể tỷ lệ thai phụ cần thực hiện các thủ thuật xâm lấn không cần thiết.
TẠI SAO NÊN LÀM NIPT Ở TUẦN THAI THỨ 10
Fetal fraction (FF) là tỷ lệ của cfDNA so với tất cả cfDNA lưu hành trong huyết tương của mẹ. Trong xét nghiệm NIPT, FF là một thông số quan trọng ảnh hưởng đến độ chính xác của NIPT. [8]
Nghiên cứu chỉ ra tỷ lệ cfDNA tự do của thai nhi trong máu mẹ bị ảnh hưởng bởi rất nhiều yếu tố trong đó có yếu tố từ mẹ bao gồm: chỉ số BMI của mẹ, ngoài ra tuổi mẹ cũng là một yếu tố ảnh hưởng đến FF. Thông số FF giữa mang thai thực hiện biện pháp hỗ trợ sinh sản và mang thai tự nhiên được nghiên cứu gần đây cũng cho thấy sự khác biệt. Ngoài ra FF bị ảnh hưởng lớn nhất bởi các yếu tố bào thai chính là tuổi thai tại thời điểm lấy máu.
Mặc dù ADN tự do của bào thai (cff ADN) xuất hiện từ tuần thai rất sớm nhưng cho tới tuần thứ 10, lượng ADN tự do mới được đánh giá là đảm bảo độ ổn định cũng như kết quả xét nghiệm NIPT được chính xác.
=> Do đó nếu thực hiện NIPT trước tuần thứ 10, kể cả vào tuần thai thứ 9 thì cũng gặp phải nguy cơ hàm lượng FF quá thấp, dẫn tới ko đạt giới hạn phát hiện của xét nghiệm NIPT. Từ đó dẫn tới không thể đọc được kết quả và yêu cầu cần lấy lại mẫu.
Một số trường hợp khác khi lấy mẫu ở tuần thai quá sớm, mặc dù vẫn đưa ra được kết quả nhưng ở sát ngưỡng cũng sẽ làm giảm độ chính xác của xét nghiệm. Như chúng ta đã biết đối với thai phụ thì việc lấy lại mẫu xét nghiệm cũng như kết quả ở sát ngưỡng hay ở trạng thái nghi ngờ sẽ làm ảnh hưởng đến tâm lý và sức khỏe vô cùng nặng nề. [9]
Nghiên cứu phân tích xác định hàm lượng cfDNA thực hiện xét nghiệm NIPT trên 16,843 thai phụ cho thấy: Tỷ lệ các trường hợp có cffDNA ≥4% tăng nhanh trước tuần thai thứ 10 và không tăng đáng kể từ tuần thứ 10 trở đi. Khoảng 92% của tất cả huyết tương mẹ có cffDNA > 4% từ 10 tuần.
Do đó thai phụ được khuyến cáo làm xét nghiệm NIPT từ tuần thai thứ 10 [10].
ƯU ĐIỂM VƯỢT TRỘI KHI THỰC HIỆN NIPT TẠI GENTIS
Quy trình thực hiện xét nghiệm sàng lọc trước sinh không xâm lấn NIPT tại GENTIS vô cùng đơn giản và an toàn, kết quả trả về nhanh chóng. Cụ thể gồm 4 bước sau:
Bước 1: Tư vấn về xét nghiệm NIPT
Trước khi thực hiện xét nghiệm, bác sĩ sẽ thăm khám sức khỏe của mẹ, tư vấn chi tiết để mẹ hiểu rõ xét nghiệm NIPT phát hiện được thai nhi mắc những hội chứng rối loạn di truyền nào.
Bước 2: Lấy mẫu máu
Bác sĩ tiến hành thu lấy 7 - 10ml máu tĩnh mạch tay mẹ. Sau đó, mẫu máu được chuyển đến phòng thí nghiệm để kiểm tra và phân tích.
Bước 3: Phân tích mẫu máu
DNA của thai nhi trong mẫu huyết tương của mẹ được phân tách, sau đó phân tích để phát hiện những bất thường về nhiễm sắc thể.
Bước 4: Trả kết quả và tư vấn sau xét nghiệm.
GENTIS tự hào là một trong những đơn vị hàng đầu tại Việt Nam trong lĩnh vực Phân tích di truyền. Đối với xét nghiệm NIPT, GENTIS là đối tác được chuyển giao toàn bộ công nghệ NIPT của Illumina vào năm 2018, xuyên suốt hành trình phát triển GENTIS không ngừng cải tiến tối ưu sản phẩm để mang lại xét nghiệm NIPT chất lượng nhất cho người Việt:
- Độ chính xác cao (>99%)
- Các gói xét nghiệm đa dạng
- Thời gian trả kết quả nhanh
- Chi phí hợp lý
>> Xem thêm bài viết:
TÀI LIỆU THAM KHẢO:
- Lun FM, Chiu RW, Chan KC et al (2008). Microfluidics digital PCR reveals a higher than expected fraction of fetal DNA in maternal plasma.Clin Chem, 54(10), 1664-72.
- Lo YM, Corbetta N, Chamberlain PF et al (1997). Presence of fetal DNA in maternal plasma and serum. Lancet, 350, 485-7.
- Hahn S, Huppertz B, Holzgreve W (2005). Fetal cells and cell free fetal nuleic acids in maternal blood: new tools to study abnormal placentation? Placenta.
- Wright CF, Burton H (2009). The use of cell-free fetal nucleic acids in maternal blood for non-invasive prenatal diagnosis. Hum Reprod Update, 15(1), 139-151
- Chan KC, Zhang J, Hui AB et al (2004). Size distributions of maternal and fetal DNA in maternal plasma. Clin Chem, 50, 88-92.
- Suzumori N, Ebara T, Yamada T et al (2016). Fetal cell-free DNA fraction in maternal plasma is affected by fetal trisomy. J Hum Genet, 61, 647-52
- Bianchi DW, Parker RL, Wentworth J et al. (2014). DNA Sequencing versus Standard Prenatal Aneuploidy Screening. New England Journal of Medicine, 370, 799-808.
- Deng, Cechuan, and Shanling Liu. “Factors Affecting the Fetal Fraction in Noninvasive Prenatal Screening: A Review.” Frontiers in pediatricsvol. 10 812781. 27 Jan. 2022, doi:10.3389/fped.2022.812781
- Rolnik, D L et al. “Association between fetal fraction on cell-free DNA testing and first-trimester markers for pre-eclampsia.” Ultrasound in obstetrics & gynecology : the official journal of the International Society of Ultrasound in Obstetrics and Gynecologyvol. 52,6 (2018): 722-727. doi:10.1002/uog.18993
- Zhou, Yang, et al. "Analysis of cell-free fetal DNA in 16,843 pregnant women from a single center in China using targeted sequencing approach." Placenta122 (2022): 18-22.


-370x207.jpg)
-370x207.jpg)
-370x207.jpg)






