| World Journal of Pharmaceutical Research SJIF Impact Factor 5.990 Volume 4, Issue 10, 191-201. Review Article. ISSN 2277– 7105 |
Đột biến gen prothrombin (đột biến G20210)
Prothrombin là một loại protein trong máu cần thiết để máu đông và còn được gọi là yếu tố II. Là một loại protein phụ thuộc vào vitamin K được tổng hợp trong gan và tuần hoàn với thời gian bán hủy khoảng 3-5 ngày. Cục máu đông bao gồm sự kết hợp của các tiểu cầu trong máu và mạng lưới của protein fibrin làm đông máu. Prothrombin là một protein đông máu cần thiết để tạo thành fibrin. Nếu ai đó có quá ít prothrombin, người đó có xu hướng chảy máu. [6]
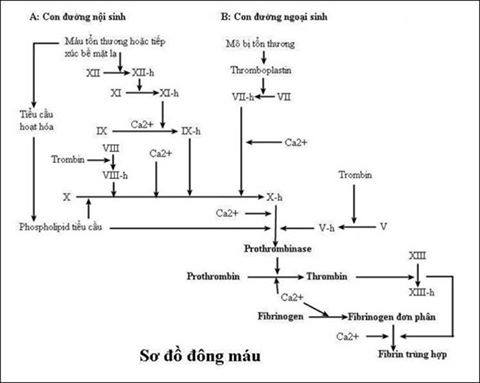
Đột biến gen prothrombin (G20210A) có liên quan đến tăng nguy cơ huyết khối và đây là yếu tố nguy cơ dễ nhận biết nhất đối với huyết khối tĩnh mạch và trên thực tế là khiếm khuyết di truyền phổ biến thứ hai đối với huyết khối di truyền, trong đó yếu tố V Leiden là yếu tố phổ biến nhất. Đây là một rối loạn tính trạng trội trên NST thường, với các dị hợp tử có nguy cơ hình thành huyết khối cao hơn 3 đến 11 lần ở cả nam và nữ và cho mọi nhóm tuổi. Mặc dù đồng hợp tử rất hiếm, nhưng việc thừa kế hai alen 20210A sẽ làm tăng nguy cơ hình thành huyết khối. [1]
Sự đột biến dẫn đến tăng lượng thrombin lưu thông trong dòng máu của người đó. Cơ chế chính xác mà đột biến gen prothrombin dẫn đến tình trạng huyết khối là không rõ ràng. Người ta cho rằng lượng prothrombin tuần hoàn tăng lên tạo ra một bàn đạp để bắt đầu quá trình đông máu và trong một số trường hợp có thể bị mất kiểm soát quá trình đông máu. Đột biến gen prothrombin (PT) được báo hiệu bởi một khiếm khuyết trong yếu tố đông máu II ở vị trí G20210A và gen prothrombin của người kéo dài 21 kb trên nhiễm sắc thể 11p11-q12 và bao gồm 14 exon và 13 intron, chiếm 90% trình tự. Đột biến này xảy ra do thay thế nucleotide G thành A ở vị trí nucleotide 20210 trong gen prothrombin. Tỷ lệ phổ biến được báo cáo ở châu Âu là khoảng 2% đến 6% và nguy cơ huyết khối tĩnh mạch đối với người mang gen dị hợp tử cao gấp ba lần dân số bình thường. [7] Nhiều nghiên cứu gần đây đã chỉ ra rằng đột biến G20210A có liên quan đến sảy thai liên tiếp và các nghiên cứu khác cho thấy tỷ lệ đột biến G20210A rất hiếm ở nhóm phụ nữ này. [8, 9]
Yếu tố V Leiden
Yếu tố V là một trong những yếu tố đông máu cần thiết trong quá trình đông máu. Dạng hoạt động là yếu tố Va, hoạt động như một đồng yếu tố cho phép yếu tố X kích thích chuyển đổi prothrombin thành thrombin. Thrombin sau đó có thể phân cắt fibrinogen thành fibrin và cục máu đông fibrin được hình thành. Protein C hoạt hóa là một chất chống đông máu tự nhiên, nó hạn chế mức độ đông máu bằng cách phá hủy yếu tố V và giảm sự hình thành thêm thrombin. Đột biến yếu tố V Leiden (FVL) (được đặt theo tên của trường đại học Hà Lan nơi phát hiện đột biến này) là một đột biến điểm trong gen tạo ra yếu tố đông máu V. Nó có tính di truyền trội trên NST thường và là nguyên nhân phổ biến nhất của bệnh huyết khối di truyền đột biến của yếu tố V Leiden gây ra kháng protein C, dẫn đến tăng huyết khối cả ở tĩnh mạch và động mạch xoắn của nhau thai. [10] Mối liên quan giữa đột biến FVL và sảy thai liên tiếp dường như mạnh hơn đối với nhóm sảy thai 3 tháng giữa không tái diễn so với nhóm sảy thai sớm tái diễn. [11]
Phụ nữ có yếu tố V Leiden có nguy cơ đông máu tăng đáng kể trong thai kỳ (và khi dùng thuốc tránh thai có chứa estrogen hoặc thay thế hormone) dưới dạng huyết khối tĩnh mạch sâu và thuyên tắc phổi. Họ cũng có thể có nguy cơ bị tiền sản giật, có thể tăng nguy cơ trẻ sơ sinh nhẹ cân, có thể tăng nguy cơ sảy thai và thai chết lưu do đông máu trong nhau thai, dây rốn hoặc bào thai (đông máu thai nhi có thể phụ thuộc vào việc em bé có được thừa hưởng gen) hoặc ảnh hưởng của hệ thống đông máu có thể có đối với sự phát triển của nhau thai. [12]
Thiếu hụt methylene tetrahydrofolate reductase
Methylene tetrahydrofolate reductase (MTHFR) là một trong những enzyme điều chỉnh chính trong quá trình chuyển hóa của homocysteine, xúc tác quá trình giảm 5, 10-methylenetetrahydrofolate thành 5-methyltetrahydrofolate. [13]
Gen MTHFR tạo ra một enzym gọi là methylene tetrahydrofolate reductase và đột biến trong gen gây ức chế sản xuất enzym này, dẫn đến tăng homocystinemia, là mức độ tăng cao của enzym homocysteine có trong huyết tương. Khi cơ thể thiếu men methylene trahydrofolate reductase, khả năng hấp thụ folate, chẳng hạn như axit folic, sẽ bị ức chế. Axit folic và B9 đều cần thiết cho sự phát triển và sức khỏe của thai nhi. Do người mẹ bị MTHFR không có khả năng chuyển hóa axit folic và vitamin B9 một cách hiệu quả, chứng rối loạn này có liên quan đến một loạt các biến chứng thai kỳ như dị tật bẩm sinh. Nồng độ homocysteine tăng cao có liên quan đến bệnh nhau thai, tiền sản giật và sảy thai liên tiếp. [15]
Các đột biến trong gen MTHFR dẫn đến giảm hoạt động của enzym và tăng procystinemia, gây ra sự kết tập tiểu cầu thông qua việc thúc đẩy tổn thương oxy hóa nội mô. Mặc dù có một số đột biến trong gen MTHFR nhưng đột biến C677T và A1298C là hai đột biến phổ biến nhất. [16] Các đa hình đơn nucleotide (SNP) trong các con đường trao đổi chất, điều chỉnh các enzym như MTHFR, được coi là yếu tố nguy cơ của bệnh huyết khối. MTHFR là enzym quan trọng trong quá trình chuyển hóa folate, methionine và homocysteine. Những xáo trộn trong hoạt động MTHFR có thể là nguyên nhân làm tăng nồng độ homocysteine trong huyết thanh. Tăng homocysteine trong máu là một yếu tố nguy cơ đối với những thay đổi trong quá trình đông máu thông qua ảnh hưởng trực tiếp gây độc tế bào nội mạc, hình thành xơ vữa, hoạt hóa yếu tố đông máu V và VII, tăng mức độ thrombin, kết tập tiểu cầu và xu hướng hình thành huyết khối tĩnh mạch. [17]
Chất ức chế plasminogen hoạt hóa 1 (PAI1)
Chất ức chế plasminogen hoạt hóa-1 là chất ức chế chính của chất hoạt hóa plasminogen mô (tPA) và chất hoạt hóa plasminogen urokinase (uPA), những yếu tố hoạt hóa plasminogen và do đó làm tiêu sợi huyết. Chất ức chế plasminogen hoạt hóa 1 (PAI-1) ức chế chất hoạt hóa plasminogen (u-PA và t-PA) bằng cách hình thành phức hợp bền vững được endocytosed thông qua cơ chế phụ thuộc thụ thể lipoprotein mật độ thấp. PAI-1 lưu thông trong huyết tương và tiềm ẩn trong tiểu cầu nhưng cũng được tiết ra và lắng đọng vào chất nền bởi một số tế bào, tham gia vào quá trình sửa chữa mô.
Biểu hiện PAI 1 nội mô được điều chỉnh bởi tính đa hình 4G/5G trong promoter PAI-1- có độ dài 675 bp từ vị trí bắt đầu phiên mã. Nồng độ angiotensin II trong huyết tương cũng ảnh hưởng đến sự biểu hiện PAI-1. Đồng hợp tử đối với alen 4G của gen PAI-1 làm tăng nguy cơ biến cố thai kỳ, dẫn đến sinh non, thai chậm phát triển trong tử cung, sảy thai và thai chết lưu. [26]
Số liệu thống kê tại GENTIS
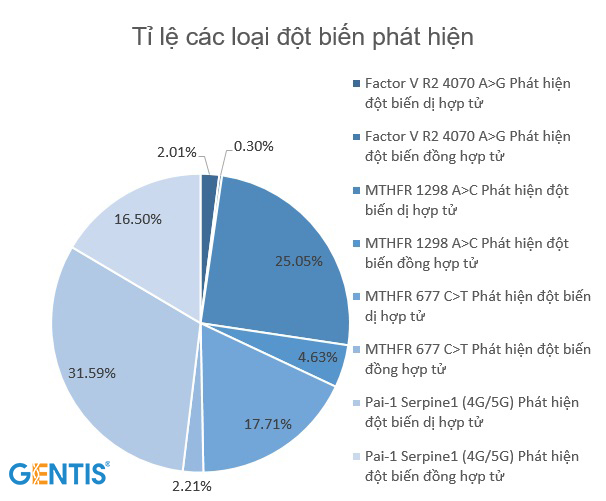
Thống kê về tỉ lệ đột biến Thrombophilia thường gặp trên 590 đối tượng hiếm muộn từ các Trung tâm Hỗ trợ sinh sản và thực hiện xét nghiệm Thrombophilia di truyền tại GENTIS từ 01/01-31/12/2020, cho thấy kết quả như sau (Hình 1,2):
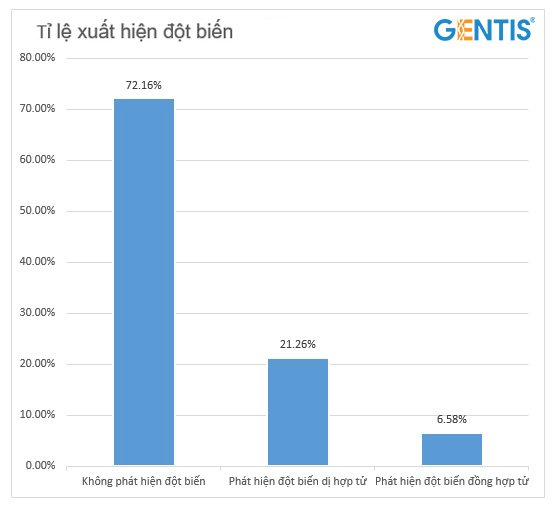
Tỉ lệ phát hiện ít nhất 1 đột biến Thrombophilia di truyền chiếm 27,84% số bệnh nhân.
Trong đó số các loại đột biến phát hiện, đột biến chủ yếu thường gặp là PAI 1 (31,59 % đột biến dị hợp tử và 16,5 % đột biến đồng hợp tử) và MTHFR (25,05 % dị hợp tử MTHFR 1298 A>C; 4.63% dị hợp tử đồng hợp tử MTHFR 1298 A>C; 17,71% dị hợp tử MTHFR 677 C>T; 2,21 % đồng hợp tử MTHFR 677 C>T).
Đột biến FV R2 4070 A>G xuất hiện với tỉ lệ 2,01 % dạng dị hợp tử và 0,3 % dạng đồng hợp tử. Không phát hiện đột biến đồng hợp tử hay dị hợp tử đối với đột biến FVL 1691 G>A, và Prothrombin FII 20210 G>C.
Bệnh huyết khối do di truyền hoặc mắc phải đã được chứng minh là nguyên nhân chính gây ra sảy thai liên tiếp, những bệnh nhân bị sảy thai nhiều lần nên được đánh giá về rối loạn đông máu, ngay cả khi không có dấu hiệu lâm sàng vì đã có một số nghiên cứu kết luận rằng nhiều phát hiện nguyên nhân máu khó đông dương tính mà không bất kỳ dấu hiệu lâm sàng nào. Đánh giá này có thể hữu ích trong việc cải thiện chăm sóc sản phụ khoa ở phụ nữ bị sảy thai liên tục và có kiến thức chính xác về tất cả các biến chứng đáng kể ở những phụ nữ này liên quan đến bệnh huyết khối và lập kế hoạch chẩn đoán và điều trị các tình trạng này.
Tài liệu tham khảo
- Khan, Salwa, and Joseph D. Dickerman. "Hereditary thrombophilia." Thromb J4, 2006; 15: 15.
- Reznikoff‐Etiévant, M. F., et al. "Factor V Leiden and G20210A prothrombin mutations are risk factors for very early recurrent miscarriage." BJOG: An International Journal of Obstetrics & Gynaecology, 2001; 108(12): 1251-1254.
- Benedetto C, Marozio L, Tavella AM, Salton L, Grivon S, Di Giampaolo F. Coagulation disorders in pregnancy: acquired and inherited thrombophilias. Ann N Y Acad Sci, 2010; 1205: 106-17.
- Kujovich, Jody Lynn. "Factor v Leiden thrombophilia." Genetics in Medicine, 2011; 13(1): 1-16.
- Battinelli, Elisabeth M., Ariela Marshall, and Jean M. Connors. "The role of thrombophilia in pregnancy." Thrombosis, 2013; 2013.
- Elizabeth A. Varga, MS and Stephan Moll. Prothrombin 20210 Mutation. American heart association, 2013; 110: e15-e18.
- Poort SR, Rosendaal FR, Reitsma PH, Bertina RM. A common genetic variation in the 3’ untranslated region of the prothrombin gene is associated with elevated plasma prothrombin levels and an increase in venous thrombosis. Blood, 1996; 88: 3698-3703.
- Li, Wei. "Stress and Recurrent Miscarriage," 2010.
- Babker, Asaad Mohammed Ahmed Abd Allah, and Fath EIrahman Mahdi Hassan Gameel. "Molecular Characterization of Prothrombin G20210A gene Mutations In pregnant Sudanese women with spontaneous recurrent abortions."Rawal Medical Journal, 2015; 40(2): 207-209.
- van Mens, Thijs E., Marcel Levi, and Saskia Middeldorp. "Evolution of factor V Leiden." Thromb Haemost, 2013; 110(1): 23-30.
- Robertson L, Wu O, Langhorne P, Twaddle S, Clark P, Lowe GD, et,al. Thrombophilia in pregnancy: a systematic review. Br J Haematol, 2006; 132: 171-196.
- Rodger MA, Paidas M, McLintock C et al. "Inherited thrombophilia and pregnancy complications revisited". Obstetrics and Gynecology, August 2008; 112(2 Pt 1): 320–24.
- Forges, T., Monnier-Barbarino, P., Alberto, J.M., GuéantRodriguez, R.M., Daval, J.L., and J.L. Guéant Impact of folate and homocysteine metabolism on human reproductive health. Hum. Reprod. Update, 2007; 13: 225-238.
- Ivy A, Alan A, Louis MA The 5, 10 methylenetetrahydrofolate reductase C677T mutation and risk of fetal loss: a case series and review of the literature. Thromb J, 2007; 5: 17.
- Foka, Z. J., et al. "Factor V Leiden and prothrombin G20210A mutations, but not methylenetetrahydrofolate reductase C677T, are associated with recurrent miscarriages." Human Reproduction, 2000; 15(2): 458-462.
- Mtiraoui, N., et al. "Methylenetetrahydrofolate reductase C677T and A1298C polymorphism and changes in homocysteine concentrations in women with idiopathic recurrent pregnancy losses." Reproduction, 2006; 131(2): 395-401.
- Spiroski, Igor, et al. "Association of methylenetetrahydrofolate reductase (MTHFR-677 and MTHFR-1298) genetic polymorphisms with occlusive artery disease and deep venous thrombosis in Macedonians." Croatian medical journal, 2008; 49(1): 39.
- Seval Ozgu-Erdinc, Cihan Togrul, Ayla Aktulay, Umran Buyukkagnici, Elif Gul Yapar Eyi, and Salim Erkaya, “Factor XII (Hageman) Levels in Women with Recurrent Pregnancy Loss,” Journal of Pregnancy, vol. 2014, Article ID 459192, 3 pages, 2014. doi:10.1155/2014/459192.
- Mariano, Martin-Loeches, et al. "Coagulation Factor XII Congenital Deficiency in Women with Recurrent Miscarriage." International Journal of Clinical Medicine, 2011; 2(04): 469.
Ngọc Hà - GENTIS HN


-370x207.jpg)
-370x207.jpg)
-370x207.jpg)






