-
- 1800 2010
- VN

Tin chuyên ngành
Array
(
[0] => stdClass Object
(
[id] => 850
[id_crawler] =>
[category_product] => NULL
[thumbnail] => tin-tuc/2022/di-tat-thai-nhi-moc-duoi.jpg
[album] =>
[url_video] =>
[is_status] => 1
[is_featured] => 0
[is_form] => 0
[displayed_time] => 0000-00-00
[program] => 0
[number] => 1
[viewed] => 0
[type] =>
[type_career] =>
[level] =>
[address] =>
[address_career] =>
[expiration_time] => 0000-00-00
[created_time] => 2022-03-07 19:38:05
[updated_time] => 2022-05-09 11:47:16
[files] =>
[salary] =>
[time] =>
[created_by] => 64
[is_table_content] => 1
[language_code] => vi
[slug] => di-tat-thai-nhi-moc-duoi
[title] => 2 loại dị tật thai nhi mọc đuôi & Cách phát hiện sớm, chính xác
[description] => Dị tật trẻ sơ sinh mọc đuôi hay còn đuôi là một dị tật bẩm sinh rất hiếm gặp. Theo thống kê, có dưới 50 ca được báo cáo cho tới nay. Vậy nguyên nhân trẻ dị tật mọc đuôi là gì, cách phát hiện và hướng điều trị như thế nào, mời mẹ tham khảo câu trả lời trong bài viết dưới đây.
[content] =>
1. 2 loại dị tật thai nhi mọc đuôi phổ biến
Hiện nay, có 2 loại dị tật thai nhi mọc đuôi phổ biến là thai nhi còn đuôi sau sinh và hội chứng nàng tiên cá.
1.1. Thai nhi còn đuôi sau khi sinh
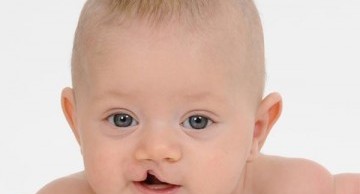
Đây là dị tật có thể quan sát bằng mắt thường sau sinh với phần thịt thừa dài, hình dạng rất thay đổi nằm giữa 2 khe mông của trẻ hoặc đôi khi nằm tại vị trí ngang đốt xương cùng cuối cùng của trẻ.
Tỷ lệ gặp phải dị tật này là vô cùng hiếm. Tại Việt Nam mới chỉ có một vài ca trẻ mới sinh còn đuôi được báo cáo.

Một ca trẻ sơ sinh có đuôi dài 12 cm được báo cáo tại Ấn Độ
Nguyên nhân dẫn tới trẻ có dị tật này chưa được làm rõ. Tuy nhiên, theo các nhà khoa học, khoảng thời gian từ tuần thứ 4 tới tuần 8, bào thai sẽ tồn tại đuôi và rụng đi. Nếu trong thời gian này thai nhi chịu tác động hóa học, sinh học chưa xác định từ môi trường thông qua cơ thể mẹ, khả năng còn đuôi sau sinh là có thể xảy ra.
Tật còn đuôi có thể chẩn đoán thông qua siêu âm 2D thông thường với bác sĩ siêu âm có kinh nghiệm.
Điều trị dị tật này cũng vì thế chia làm 2 phương pháp:
- Nếu phần đuôi không có tế bào thần kinh tủy sống: Có thể cắt bỏ được bằng phẫu thuật. Sau cắt đuôi trẻ không bị ảnh hưởng gì đến thể chất và trí tuệ.
- Nếu khối thừa là thoát vị màng não tủy: Phẫu thuật cắt bỏ sẽ ảnh hưởng đến phần tủy sống bình thường phía trên. Trường hợp dị tật đánh giá là nhẹ có thể điều trị, trẻ có cơ may không bị liệt và sống bình thường, tuy nhiên hầu hết sẽ có di chứng về tâm thần.
Dị tật thai nhi còn đuôi không ảnh hưởng nhiều đến sức khỏe của trẻ, chỉ ảnh hưởng chủ yếu tới thẩm mỹ và sự tự tin của trẻ. Do đó, cha mẹ cần được phát hiện và điều trị sớm để không ảnh hưởng đến tâm lý khi bé lớn lên.

Trẻ sinh ra có vùng thịt thừa sau lưng khiến nhiều người liên tưởng tới trẻ mọc đuôi
1.2. Hội chứng nàng tiên cá (sirenomelia)
Đây là dị tật vô cùng hiếm, biểu hiện trẻ sinh ra hai chân dính liền vào nhau tạo thành đuôi và không thể đi lại được.
Hiện nay, chưa ghi nhận trẻ gặp phải hội chứng này tại Việt Nam. Trên thế giới tỷ lệ trẻ mắc hội chứng sirenomelia được báo cáo là 1/100.000, được ghi nhận tại Trung Quốc, Mỹ và một số nước phương Tây. Trẻ trai thường gặp hơn trẻ gái.
Mẹ mắc đái tháo đường và cocain được cho là liên quan tới hội chứng đuôi cá này. Một số giả thiết cho rằng hội chứng sirenomelia là do thai nhi thiếu máu cấp cho chi dưới trong quá trình phát triển, số khác cho rằng đã có bất thường từ môi trường ảnh hưởng tới sự phát triển trung bì đuôi giai đoạn ngày 28 - 32 sau thụ tinh. Các giả thuyết này hiện nay đều chưa được kiểm chứng.
Hội chứng nàng tiên cá rất đặc biệt và có thể chẩn đoán sớm từ tuần thứ 14 thông qua siêu âm.
Dị tật này thường gây sẩy thai tự nhiên và tử vong chu sinh với tỷ lệ từ ⅓ - ½ trẻ. Nếu trẻ được sinh ra với dị tật dính hai chi dưới còn sống, điều trị thường hướng tới làm giảm các triệu chứng chèn ép nội tạng, phẫu thuật tạo hình và phục hồi chức năng cơ quan cần thiết duy trì sự sống. Một số trường hợp đủ cơ quan và mạch máu nuôi, trẻ có thể được phẫu thuật tách rời chi và tập đi với dụng cụ trợ giúp.
Theo thống kê [1], có 3 trường hợp mắc chứng sirenomelia sống qua 10 tuổi được ghi nhận, trong đó có trường hợp sống tới năm 27 tuổi.

Em bé mắc hội chứng nàng tiên cá do hai chi dưới dính liền
2. Dấu hiệu nhận biết dị tật thai nhi mọc đuôi
Bằng cảm nhận, mẹ không thể phát hiện dị tật thai nhi mọc đuôi vì hiện nay chưa tìm ra mối liên hệ và nguyên nhân phát sinh dị tật này. Mặt khác, các dị tật bẩm sinh thường xảy ra vào giai đoạn sớm như các trung tâm hóa xương chính phát triển ở tất cả các xương dài của các chi vào tuần thứ 12 của tuổi thai. Giai đoạn sớm này thậm chí nhiều sản phụ còn chưa phát hiện mình có thai.
Sau 3 tháng đầu, siêu âm đã cho phép đánh giá gần như toàn bộ hình thái của thai nhi. Đây cũng là biện pháp sàng lọc đơn giản nhất mẹ có thể thực hiện để chẩn đoán dị tật thai nhi mọc đuôi.

Siêu âm quý hai giúp tầm soát trẻ sinh ra mắc dị tật còn đuôi chưa rụng
Xem thêm: Dị tật thai nhi xuất hiện khi nào? 3 Thời điểm phát hiện QUAN TRỌNG
3. Cách phát hiện dị tật thai nhi mọc đuôi chính xác nhất
Với dị tật hình thái như dị tật bẩm sinh còn đuôi, chỉ có siêu âm quý 2 là phương pháp có thể khảo sát và chẩn đoán được trước sinh.
Quy trình siêu âm sẽ được bác sĩ đánh giá lần lượt sự phát triển của các xương, cấu trúc cơ quan từ đầu tới chân, nhằm mục đích không bỏ sót dị tật, trong đó có hội chứng Sirenomelia và hội chứng trẻ có đuôi.
Ngoài dị tật mọc đuôi và trên thực tế đây là một trong những dị tật bẩm sinh hiếm gặp, thai nhi còn có nguy cơ mắc các dị tật bẩm sinh thường gặp hơn rất nhiều nguyên nhân do bất thường số lượng NST. Điển hình như Down, Turner, hội chứng tiếng mèo kêu Cri-du-chat,... Các dị tật này được phát hiện sớm nhất thông qua sàng lọc với NIPT Illumina không xâm lấn từ tuần thứ 10 sau khi thụ tinh.
NIPT của GENTIS thực hiện trên công nghệ Illumina - Mỹ, giúp sàng lọc chính xác >99% các dị tật bẩm sinh thường gặp liên quan tới đột biến cấu trúc, số lượng NST.

GENTIS trao cho mẹ cơ hội hiểu đúng về thai nhi với xét nghiệm sàng lọc NIPT Illumina GenEva
Mọi mẹ bầu trên thế giới nói chung và tại Việt Nam nói riêng đều được Bộ Y Tế nước cư trú khuyến cáo nên sàng lọc trước sinh thai nhi để phòng sinh ra những em bé mang dị tật bẩm sinh.
4. Mẹ cần làm gì khi được chẩn đoán thai nhi bị dị tật mọc đuôi?
Điều cần nhớ khi phát hiện con có dị tật còn đuôi là mẹ cần bình tĩnh lắng nghe lời khuyên của bác sĩ. Đây là dị tật hiếm nhưng không nguy hiểm. Một khi được làm MRI và loại trừ dị tật ống thần kinh, em bé sinh ra có cơ hội rất lớn được phát triển như một đứa trẻ bình thường sau khi phẫu thuật cắt đuôi.
Trên thực tế, có những em bé sinh ra với dị tật thai nhi mọc đuôi đã được phẫu thuật sớm để trở lại cuộc sống bình thường như bao đứa trẻ khác.
Dưới đây là 1 số lưu ý giúp mẹ bầu có thai kỳ khỏe mạnh, tránh dị tật thai nhi mọc đuôi:
- Chế độ ăn uống khoa học: Bổ sung acid folic trước khi mang thai 1 tháng và sau khi có thai liên tục. Nếu có tiền sử con mắc dị tật ống thần kinh, hàm lượng acid folic được khuyến cáo là từ 4 - 5mg/ngày.
- Không sử dụng chất kích thích: Những mối liên quan của rượu, bia, thuốc lá tới tỷ lệ sinh con mang dị tật bẩm sinh tuy chưa rõ ràng nhưng phòng tránh là điều mọi nhân viên y tế đều khuyến cáo.
- Chỉ sử dụng thuốc khi có chỉ định của bác sĩ: Các thuốc đang sử dụng bất kể thuốc kê đơn nào (Có chữ R trên bao bì) đều cần được thông qua ý kiến của bác sĩ sản khoa của mẹ. Nguy cơ dị tật luôn tiềm ẩn khiến tờ hướng dẫn sử dụng của mọi loại thuốc đều có yêu cầu thận trọng khi dùng trên phụ nữ có thai.
- Khám thai định kỳ: Theo chỉ định của bác sĩ hoặc 4 tuần/lần nhằm theo dõi sát những thay đổi của thai nhi để kịp thời điều chỉnh về các giới hạn bình thường, giúp em bé phát triển đúng hướng và khỏe mạnh nhất.

Bổ sung acid folic hay vitamin B9 là phương pháp hiệu quả nhất giúp phòng ngừa các dị tật bẩm sinh nghiêm trọng
Bài viết trên đã truyền đạt tới mẹ những thông tin về 2 loại dị tật mọc đuôi hiếm gặp ở trẻ. Hy vọng mẹ có cái nhìn toàn diện hơn về sàng lọc sớm dị tật bẩm sinh cho thai nhi cũng như có những quyết định đúng đắn dựa trên những lời khuyên có tính chuyên môn từ bác sĩ. Nếu có thắc mắc về sàng lọc sớm trước sinh ở đâu và bằng hình thức nào, mẹ vui lòng liên hệ với GENTIS qua hotline 0988 00 2010 để được tư vấn nhé!
1. Cách đọc kết quả sàng lọc trước sinh Double test
Xét nghiệm sàng lọc trước sinh Double test thực hiện trên mẫu máu tĩnh mạch của mẹ bầu vào tuần thứ 11 - 13 của thai kỳ qua việc định lượng 2 chỉ số:
- Nồng độ β - hCG tự do (free beta-human chorionic gonadotropin).
- PAPP - A (pregnancy associated plasma protein A) có trong máu của thai phụ.
Giá trị bình thường của các thông số β-hCG tự do và PAPP-A máu thai phụ sau khi hiệu chỉnh đều bằng 1 MoM. Thai nhi có nguy cơ với hội chứng Down, hội chứng Trisomy 13 và trisomy 18 nếu:
- β-hCG tự do trong máu < 0,4 hoặc > 2,5 MoM
- PAPP - A < 0,4 MoM
Cùng với đó, bác sĩ sẽ chỉ định thêm siêu âm để đo độ mờ da gáy, giúp tăng mức độ chính xác đánh giá nguy cơ hội chứng Down.

Double test định lượng β - hCG tự do và PAPP - A trong máu mẹ
Xem thêm: 8 điều mẹ cần biết về Sàng lọc trước sinh bệnh Down
Nguy cơ của thai được đánh giá dựa theo các ngưỡng, để hiểu rõ hơn về cách đọc kết quả, mẹ tham khảo bảng hướng dẫn sau.
|
Dị tật |
Ngưỡng nguy cơ |
Cách hiểu kết quả |
|
Hội chứng Down |
Ngưỡng nguy cơ của thai nhi với nguy cơ mắc hội chứng Down là 1/250 |
|
|
Hội chứng down theo tuổi mang thai của mẹ |
Ngưỡng nguy cơ của thai nhi với hội chứng Down theo tuổi mang thai của mẹ là 1/250 |
|
|
Hội chứng trisomy 13/18 |
Ngưỡng nguy cơ với hội chứng Trisomy 13/18 (Edwards, Patau) ở khoảng 1/100 |
|
Ví dụ về bảng kết quả dị tật thai nhi double test:
|
Dị tật |
Ngưỡng nguy cơ |
Nguy cơ của thai |
Giải thích |
|
Hội chứng Down |
1/ 250 |
1/ 526 |
Trong khoảng 526 thai phụ giống như bạn, có thể có 1 thai phụ sinh con bị Down, 525 thai phụ sinh con không bị Down |
|
Hội chứng Down theo tuổi mang thai của mẹ |
1/250 |
1/305 |
Trong khoảng 305 thai phụ giống như bạn, có thể có 1 thai phụ sinh con bị Down |
|
Hội chứng Trisomy 13/18 |
1/100 |
< 1/10000 |
Trong khoảng 10000 thai phụ giống như bạn có thể có 1 thai phụ sinh con bị hội chứng Trisomy 13/18 |
Kết luận của sàng lọc này: Thai nhi có nguy cơ thấp với hội chứng Down, hội chứng Trisomy 13/18.

Mẫu phiếu kết quả xét nghiệm Double test
2. Xét nghiệm double test có chính xác không?
Thầy thuốc nhân dân - PGS.TS. BS Nguyễn Duy Ánh, giám đốc bệnh viện Phụ Sản Hà Nội cho biết phương pháp này có độ chính xác chỉ khoảng 70%. Kết quả sàng lọc trước sinh Double test có ý nghĩa sàng lọc xem thai nhi có nguy cơ cao hay thấp mắc dị tật thai nhi hội chứng Down, Trisomy 13/18, chúng không phải là để chẩn đoán thai nhi có dị tật không.
Mặc dù độ chính xác của Double test chỉ khoảng 70%, nhưng mẹ bầu vẫn cần thực hiện xét nghiệm này để sàng lọc nguy cơ dị tật, giúp kịp thời phát hiện và làm giảm việc phải xâm lấn vào tế bào thai đối với mẹ có nguy cơ thấp.
Mẹ tham khảo thêm bài viết: Xét nghiệm double test có chính xác không?

Mẹ nên thực hiện xét nghiệm Double test vào tuần thứ 11 -13 vì lúc này sự thay đổi các chỉ số β-hCG tự do và PAPP-A là rõ rệt nhất
Để có kết quả sàng lọc trước sinh double test chính xác, mẹ cần lưu ý:
- Thời điểm xét nghiệm vào tuần 11-3: Mẹ bầu nên thực hiện vào tuần thứ 11 - 13 của thai kỳ vì đây là lúc các chỉ số β-hCG tự do và PAPP-A có sự thay đổi rõ rệt nhất. Với 2 chỉ số này, mẹ có thể xét nghiệm bất cứ lúc nào phù hợp, không cần nhịn ăn sáng và ăn kiêng.
- Địa điểm xét nghiệm uy tín: Theo nghiên cứu [1] về các yếu tố ảnh hưởng đến kết quả sàng lọc trước sinh, lựa chọn địa chỉ uy tín giúp cho kết quả có độ chính xác hơn. Vì ở các đơn vị uy tín sẽ được trang bị máy móc hiện đại, kỹ năng của kỹ thuật viên và kiến thức y khoa của bác sĩ chuyên môn có ảnh hưởng đến kết quả. Mẹ đừng quên lựa chọn cho mình đơn vị sàng lọc uy tín nhé!
Ngoài ra, mẹ cũng cần thông báo cho bác sĩ biết về các loại thuốc đang sử dụng, tiền sử bệnh tật trong gia đình đặc biệt của bố và mẹ để kết hợp chẩn đoán chính xác và nhận được lời khuyên tốt nhất từ bác sĩ.
3. Cần làm gì sau khi nhận kết quả sàng lọc trước sinh double test
Vậy sau khi có kết quả Double test, mẹ bầu cần làm gì? Câu trả lời phụ thuộc vào việc đánh giá nguy cơ như thế nào, cụ thể như sau:
- Xét nghiệm Double test cho nguy cơ thấp: Điều này có nghĩa thai nhi có nguy cơ rất thấp mắc các dị tật Down, Trisomy 13/18. Tuy nhiên, mẹ không nên chủ quan và cần theo dõi, sàng lọc các dị tật khác đúng định kỳ vì kết quả chỉ chính xác 70%, đồng thời trong quá trình phát triển thai nhi vẫn có nguy cơ gặp các biến chứng bất thường khác.
- Xét nghiệm Double test cho nguy cơ cao: Điều này có nghĩa thai nhi có nguy cơ cao mắc các dị tật như hội chứng Down, hội chứng Trisomy 13/18. Lúc này, mẹ cần bình tĩnh tham khảo tư vấn của bác sĩ để thực hiện các xét nghiệm khác nhằm đánh giá nguy cơ dị tật chính xác hơn. Bởi theo đánh giá của BS Nguyễn Duy Ánh (giám đốc bệnh viên phụ sản Hà Nội), phương pháp này chỉ chính xác khoảng 70%.

Khi được đánh giá nguy cơ cao, mẹ cần bình tĩnh, tham khảo tư vấn chuyên môn từ bác sĩ
4. Giải đáp thắc mắc liên quan đến kết quả sàng lọc double test
Để giúp mẹ hiểu rõ hơn về kết quả sàng lọc trước sinh Double test, GENTIS tổng hợp thêm một số câu hỏi thường gặp nhất. Mẹ kéo xuống để tham khảo nhé!
4.1. Kết quả sàng lọc trước sinh double test bao lâu thì có?
Kết quả sàng lọc trước sinh Double test bao lâu thì có phụ thuộc vào đơn vị thực hiện, thường từ vài giờ tới vài ngày. Mẹ có thể nhận kết quả trực tiếp tại đơn vị sàng lọc hoặc nhận gửi bản cứng về nhà, kết quả online tùy hình thức đăng ký và địa chỉ test sàng lọc.
4.2. Độ mờ da gáy thấp nhưng double test nguy cơ cao phải làm sao?
Theo ý kiến của chuyên gia y tế, nếu độ mờ da gáy thấp, mẹ vẫn nên làm thêm Double test để đánh giá chính xác hơn nguy cơ bị Down và biết thêm nguy cơ hội chứng Trisomy 13/18.
Tuy nhiên Double test chỉ đúng khoảng 70%, mẹ có thể làm xét nghiệm NIPT Illumina có độ chính xác >99% hoặc lắng nghe tư vấn của bác sĩ để chọn được phương pháp phù hợp.

Nếu muốn kết quả chính xác cao, mẹ nên thực hiện xét nghiệm NIPT tại GENTIS với độ chính xác >99%
4.3. Chỉ số papp-a bao nhiêu là bình thường?
Kết quả xét nghiệm Double Test là bình thường khi các giá trị của thông số β-hCG tự do và PAPP-A máu thai phụ bình thường, cụ thể sau khi hiệu chỉnh đều bằng 1 MoM. Với nồng độ PAPP-A < 0.4 MoM, thai nhi có nguy cơ bị hội chứng Down, Trisomy 13/18.
Kết quả sàng lọc trước sinh Double test chỉ có ý nghĩa đánh giá nguy cơ, không chẩn đoán chính xác thai nhi có gặp dị tật hay không. Vì vậy, dù kết quả thế nào, mẹ vẫn cần theo dõi và thăm khám, tuân thủ các hướng dẫn từ bác sĩ chuyên môn, tránh chủ quan hoặc lo lắng quá mức. Nếu cần tư vấn thêm, mẹ liên hệ trực tiếp tới hotline 18002010 nhé!
[content_more] => [meta_title] => Hướng dẫn chi tiết A - Z về kết quả sàng lọc trước sinh double test [meta_description] => Cách đọc kết quả double test như thế nào? Mẹ theo dõi bài viết sau để hiểu tường tận từ A đến Z về kết quả sàng lọc trước sinh Double test nhé! [meta_keyword] => kết quả sàng lọc trước sinh double test [thumbnail_alt] => kết quả sàng lọc trước sinh double test [post_id] => 847 [category_id] => 15 ) [2] => stdClass Object ( [id] => 846 [id_crawler] => [category_product] => NULL [thumbnail] => tin-tuc/2022/xet-nghiem-double-test-co-chinh-xac-khong.jpg [album] => [url_video] => [is_status] => 1 [is_featured] => 0 [is_form] => 0 [displayed_time] => 0000-00-00 [program] => 0 [number] => 1 [viewed] => 0 [type] => [type_career] => [level] => [address] => [address_career] => [expiration_time] => 0000-00-00 [created_time] => 2022-03-04 16:33:43 [updated_time] => 2022-05-09 13:59:08 [files] => [salary] => [time] => [created_by] => 64 [is_table_content] => 1 [language_code] => vi [slug] => xet-nghiem-double-test-co-chinh-xac-khong [title] => Xét nghiệm Double Test có chính xác không? 2 yếu tố ảnh hưởng [description] => Xét nghiệm Double test có chính xác không? Theo đánh giá của thầy thuốc nhân dân Nguyễn Duy Ánh (giám đốc bệnh viện Phụ Sản Hà Nội), phương pháp này có độ chính xác khoảng 70%. Vậy vì sao mẹ vẫn cần thực hiện sàng lọc Double test? Có phương pháp nào với độ chính xác cao hơn không? Để hiểu về vấn đề này, mẹ theo dõi tư vấn của GENTIS trong bài viết dưới đây! [content] =>1. Độ chính xác của phương pháp xét nghiệm double test
Xét nghiệm sàng lọc trước sinh Double test kiểm tra định lượng β-hCG tự do và PAPP-A trong máu mẹ. Hai chỉ số hóa sinh này do nhau thai tiết ra, làm thay đổi trong quá trình mang thai. Dựa vào sự bất thường về các chỉ số này, bác sĩ có thể đánh giá nguy cơ thai nhi có bị các dị tật như hội chứng Down, Edwards và Patau như sau:
- Nguy cơ mắc bệnh Down: Ngưỡng an toàn với nguy cơ mắc hội chứng Down của thai nhi và tuổi của thai phụ là 1:250, có nghĩa là:
- Thai nhi có nguy cơ thấp mắc Down: Kết quả Double test có mẫu số lớn hơn 250
- Thai nhi có nguy cơ cao mắc Down: Kết quả Double test có mẫu số nhỏ hơn 250
- Nguy cơ mắc bệnh Patau và Edward: Ngưỡng an toàn với nguy cơ mắc hội chứng này là 1:100, có nghĩa là:
- Thai nhi có nguy cơ thấp mắc bệnh Patau và Edward: Kết quả Double test có mẫu số lớn hơn 100
- Thai nhi có nguy cơ cao mắc bệnh Patau và Edward: Kết quả Double test có mẫu số nhỏ hơn 100.

Xét nghiệm Double test là kỹ thuật định lượng β-hCG tự do và PAPP-A trong máu mẹ
Xét nghiệm Double test có độ chính xác chỉ khoảng 70%, nó chỉ có ý nghĩa sàng lọc xem mẹ có nguy cơ cao hay thấp, không phải là để chẩn đoán.
Thầy thuốc nhân dân - PGS.TS. BS Nguyễn Duy Ánh, giám đốc bệnh viện Phụ Sản Hà Nội
Do đó, nếu mẹ bầu được xếp vào nhóm nguy cơ cao không có nghĩa là 100% thai nhi bị dị tật. Lúc này mẹ cần được làm thêm các sàng lọc khác để được đánh giá chính xác nguy cơ hơn như phương pháp NIPT hoặc chọc ối. Ngược lại, khi mẹ được đánh giá nguy cơ thấp không có nghĩa thai nhi 100% an toàn, mẹ vẫn phải theo dõi sức khỏe, siêu âm và thực hiện các sàng lọc định kỳ tiếp theo.
Mặc dù độ chính xác của Double test chỉ khoảng 70%, nhưng mẹ bầu vẫn cần thực hiện theo khuyến cáo vì double test giúp sàng lọc và hạn chế các tác động không cần thiết cho thai nhi có nguy cơ thấp (ví dụ phương pháp chọc ối).
2. 2 yếu tố ảnh hưởng đến độ chính xác của double test
Để có kết quả xét nghiệm Double test chính xác nhất, mẹ cần chú ý đến thời gian sàng lọc và lựa chọn được địa chỉ xét nghiệm uy tín vì:
- Thời gian sàng lọc: Kết quả sàng lọc Double test dựa trên 2 thông số là β-hCG tự do và PAPP-A. Thời điểm 11 - 13 tuần là giai đoạn vàng vì lúc này những bất thường về 2 chỉ số này là rõ ràng nhất, cụ thể:
- Nồng độ β-hCG sẽ tăng đáng kể trong 2 quý đầu nếu thai nhi mắc hội chứng Down, Patau và Edward.
- Nồng độ PAPP-A trong máu mẹ giảm ở quý I của thai kỳ nếu thai nhi mắc các hội chứng này. Trong khi đó ở thai kỳ sau 14 tuần, nồng độ PAPP-A vẫn giữ ở mức bình thường hoặc giảm nhẹ (không đáng kể) nên sẽ khó phát hiện chính xác nếu mẹ thực hiện xét nghiệm ở các tuần sau đó.
- Địa chỉ xét nghiệm: Theo đánh giá của chuyên gia y tế, kỹ thuật của nhân viên y tế và phương tiện máy móc trang bị ảnh hưởng tới kết quả, độ chính xác và sự an toàn của mẹ bầu. Do đó, mẹ cần lựa chọn các đơn vị sàng lọc double test uy tín, được cấp phép bởi cơ quan y tế, có đội ngũ chuyên gia, kỹ thuật viên với tay nghề cao và trang bị máy móc hiện đại nhất.

Xét nghiệm Double test có độ chính xác cao nhất khi mẹ thực hiện ở tuần 11 - 13
3. Phương pháp sàng lọc nào có độ chính xác cao hơn Double test?
3 phương pháp sàng lọc dị tật thai nhi được Bộ y tế khuyến cáo hiện nay là: Double test, Triple test, NIPT. Trong đó, phương pháp xét nghiệm Double test có độ chính xác thấp nhất. Để hiểu rõ hơn về độ chính xác và các sàng lọc này, mẹ kéo xuống bảng so sánh một số đặc điểm nổi bật dưới đây!
|
Double test |
Triple test |
NIPT Illumina |
|
|
Đặc điểm của phương pháp |
Kiểm tra định lượng β-hCG tự do và PAPP-A trong máu mẹ |
Đo nồng độ các protein, glycoprotein nguồn gốc bào thai, nhau thai lưu hành trong máu mẹ |
Phân tích các đoạn ADB tự do của thai nhi trong máu của mẹ |
|
Độ chính xác |
Khoảng 70% |
Khoảng 80 % |
>99% |
|
Các dị tật chẩn đoán được |
Hội chứng Down, hội chứng Edwards và hội chứng Patau |
Hội chứng Down, hội chứng Edward, dị tật ống thần kinh |
Xét nghiệm được nhiều loại dị tật khác nhau tùy thuộc mức giá, chủ yếu xét phát hiện các loại dị tật như: Hội chứng Down, hội chứng Edwards, Hội chứng Patau, nhiễm sắc thể giới tính. |
|
Giá thành |
Khoảng 400.000 đồng - 1.000.000 đồng |
Khoảng 400.000 đồng - 1.000.000 đồng |
Khoảng 3.000.000 đồng - 18.000.000 đồng |
|
Mức độ an toàn |
An toàn vì chỉ xét nghiệm máu mẹ, không xâm lấn thai nhi |
An toàn vì chỉ xét nghiệm máu mẹ, không xâm lấn thai nhi |
An toàn vì chỉ xét nghiệm máu mẹ, không xâm lấn thai nhi |
Dựa vào bảng trên mẹ bầu dễ dàng nhận thấy phương pháp NIPT có độ chính xác >99%, hơn hẳn 2 phương pháp còn lại. Vì vậy để đảm bảo kết quả chính xác nhất, mẹ nên lựa chọn sàng lọc trước sinh NIPT nếu có điều kiện. Mẹ tham khảo xét nghiệm sàng lọc NIPT tại GENTIS - địa chỉ uy tín được bác sĩ Vũ Bá Quyết ( Nguyên Giám đốc Bệnh viện Phụ sản Trung Ương) đánh giá cao và nhiều mẹ bỉm sữa review chất lượng.
Để được tư vấn nhanh và đặt lịch hẹn, mẹ liên hệ hotline: 18002010 để được GENTIS sẽ tư vấn và trả kết quả xét nghiệm nhanh chóng sau 5 ngày.

Xét nghiệm NIPT có độ chính xác >99%
4. Câu hỏi thường gặp khi làm xét nghiệm double test
Phần dưới đây, GENTIS sẽ giải đáp một số câu hỏi thường gặp khi làm xét nghiệm Double test. Mẹ theo dõi thêm để hiểu rõ hơn về xét nghiệm này nhé!
4.1. Làm Double test rồi có cần làm Triple test không?
Xét nghiệm Triple test là cần thiết phải thực hiện ở tuần 15 - 20 để phát hiện các loại dị tật: Dị tật Down, hội chứng Edward, dị tật ống thần kinh. Trong khi đó Double test không phát hiện được dị tật ống thần kinh. Vì vậy, xét nghiệm Double test ở tuần thứ 11 - 13 và Triple test ở tuần 16 -18 là 2 việc cần thiết, không được bỏ qua xét nghiệm sau dù xét nghiệm trước bình thường.
Ngoài ra, với những mẹ có nguy cơ cao khi sàng lọc Double test, mẹ cần thực hiện thêm xét nghiệm Triple test hoặc NIPT để giúp phát hiện các dị tật Down, Patau và Edward chính xác hơn.

Mẹ nên thực hiện cả 2 xét nghiệm Double test và Triple test
4.2. Xét nghiệm Double test là làm những gì?
Xét nghiệm Double test là quá trình định lượng hàm lượng β-hCG tự do và PAPP-A trong máu mẹ. Vì vậy, phương pháp này khá đơn giản, mẹ chỉ cần được lấy máu tĩnh mạch nhanh chóng sau đó đưa vào máy để kiểm tra, đánh giá.
Khi đi xét nghiệm Double test, mẹ cần thực hiện các công việc sau:
- Đăng ký đặt lịch nếu cần.
- Chuẩn bị giấy tờ, sổ theo dõi thai kỳ.
- Thăm khám và được tư vấn bởi các bác sĩ chuyên môn.
- Lấy máu tĩnh mạch.
- Siêu âm đo độ mờ da gáy để kết hợp đánh giá nguy cơ bị Down.
- Đợi bác sĩ gửi giấy kết quả trực tiếp hoặc tại nhà (tùy cơ sở).

Xét nghiệm Double test là xét nghiệm máu đơn giản
Hy vọng qua bài viết này mẹ đã tìm được câu trả lời cho câu hỏi xét nghiệm double test có chính xác không? Với độ chính xác khoảng 70%, đây là phương pháp sàng lọc được Bộ y tế khuyến cáo mẹ nên thực hiện, giúp kịp thời phát hiện dị tật và giảm tác động tiêu cực tới mẹ có nguy cơ thấp. Nếu khả năng tài chính của mẹ tốt hơn, chuyên gia khuyên mẹ nên thực hiện phương pháp NIPT (độ chính xác >99%) để yên tâm nhất. Chúc mẹ có thai kỳ khỏe mạnh nhất!
[content_more] => [meta_title] => Xét nghiệm Double Test có chính xác không? 2 yếu tố ảnh hưởng [meta_description] => Cần thực hiện Double test nhưng không biết xét nghiệm Double Test có chính xác không, mẹ đừng bỏ qua lời giải đáp từ GENTIS trong bài viết sau nhé! [meta_keyword] => xét nghiệm double test có chính xác không [thumbnail_alt] => xét nghiệm double test có chính xác không [post_id] => 846 [category_id] => 15 ) [3] => stdClass Object ( [id] => 842 [id_crawler] => [category_product] => NULL [thumbnail] => tin-tuc/2022/t2/xet-nghiem-sang-loc-truoc-sinh-double-test.jpg [album] => [url_video] => [is_status] => 1 [is_featured] => 0 [is_form] => 0 [displayed_time] => 0000-00-00 [program] => 0 [number] => 1 [viewed] => 0 [type] => [type_career] => [level] => [address] => [address_career] => [expiration_time] => 0000-00-00 [created_time] => 2022-02-28 02:55:08 [updated_time] => 2022-05-09 13:54:52 [files] => [salary] => [time] => [created_by] => 64 [is_table_content] => 1 [language_code] => vi [slug] => xet-nghiem-sang-loc-truoc-sinh-double-test [title] => Tổng hợp kiến thức về xét nghiệm sàng lọc trước sinh Double Test [description] => Xét nghiệm sàng lọc trước sinh Double test được thực hiện ở tuần thứ 11 - 13 của thai kỳ giúp phát hiện các dị tật như Down, hội chứng Edwards, Patau,... Vậy xét nghiệm này có chính xác không? Cần lưu ý gì khi thực hiện? Mẹ theo dõi bài viết này để hiểu rõ nhất về sàng lọc Double test nhé! [content] =>1. Xét nghiệm sàng lọc trước sinh double test là xét nghiệm gì?
Xét nghiệm sàng lọc trước sinh Double test là xét nghiệm kiểm tra định lượng β-hCG tự do và PAPP-A trong máu mẹ. Hai chỉ số hóa sinh này do nhau thai tiết ra, làm thay đổi trong quá trình mang thai.
Khi kết hợp sự thay đổi của các chỉ số này với độ mờ da gáy (NT), chiều dài đầu mông (CRL) của thai nhi và một số thông số khác bằng phần mềm chuyên dụng để giúp bác sĩ đánh giá nguy cơ dị tật.
Xét nghiệm này hoàn toàn không ảnh hưởng gì đến sức khỏe của thai nhi vì chỉ xét nghiệm máu mẹ, không xâm lấn vào tế bào thai.

Xét nghiệm Double test là kiểm tra định lượng β-hCG tự do và PAPP-A trong máu mẹ
2. Có cần thiết phải làm double test không?
Double test giúp phát hiện các nguy cơ như: Hội chứng Down (Trisomy 21), Edwards (Trisomy 18) và Patau (Trisomy 13). Double test là sàng lọc được các chuyên gia khuyến cáo mẹ nên thực hiện ở tuần thứ 11 - 13 của thai kỳ. Các loại dị tật này khó được phát hiện chính xác thông qua siêu âm, vì vậy kể cả mẹ có thực hiện siêu âm thai nhi bình thường vẫn cần thực hiện xét nghiệm Double test.
Tuy nhiên, mẹ đã thực hiện các loại xét nghiệm dị tật thai nhi khác như NIPT thì Double test là không cần thiết vì phương pháp NIPT đã có thể phát hiện các dị tật với độ chính xác cao hơn.
Như vậy, việc có cần làm xét nghiệm Double test hay không phụ thuộc vào từng trường hợp. Nếu mẹ chưa thực hiện xét nghiệm NIPT thì cần, còn đã xét nghiệm NIPT thì không cần thiết nữa.

Xét nghiệm sàng lọc trước sinh double test nên thực hiện ở tuần thứ 11 - 13 của thai kỳ
3. Đối tượng và thời điểm cần sàng lọc trước sinh double test
Tất cả các phụ nữ mang bầu nếu chưa thực hiện xét nghiệm NIPT đều cần làm xét nghiệm Double test ở tuần thứ 11 - 13 để kịp thời phát hiện nguy cơ dị tật thai nhi, đặc biệt với nhóm đối tượng có mức độ nghi dị tật cao như:
- Tiền sử gia đình có người từng bị dị tật thai nhi.
- Trên 35 tuổi.
- Mẹ đã hoặc đang sử dụng các loại thuốc có nguy cơ gây dị tật cao.
- Mẹ bầu mắc các bệnh như tiểu đường, nhiễm virus trong thời kỳ mang thai hoặc thường xuyên phải tiếp xúc với hóa chất, tia phóng xạ gây độc hại.
4. Xét nghiệm Double test hết bao nhiêu tiền?
Xét nghiệm Double test hết bao nhiêu tiền thuộc vào từng bệnh viện hay cơ sở y tế, các loại máy móc, dung môi dùng để kiểm tra. Thông thường, chi phí trung bình khoảng 400.000 đến 1.000.000 đồng. Trước khi lựa chọn thực hiện, bạn nên tham khảo ý kiến bác sĩ và cân nhắc về ưu nhược điểm của từng xét nghiệm để có thể đưa ra lựa chọn phù hợp nhất.
5. Xét nghiệm double test có chính xác không?
Theo đánh giá của PGS. TS. BS. Nguyễn Duy Ánh - Giám đốc Bệnh viện Phụ Sản Hà Nội, xét nghiệm double test có độ chính xác khoảng 70%. Vì vậy, kết quả sàng lọc trước sinh double test cho thấy thai nhi có dị tật không có nghĩa 100% con bạn bị dị tật. Lúc này, mẹ bầu cần thực hiện thêm những sàng lọc và xét nghiệm khác để được dự đoán chính xác hơn. Cũng theo đánh giá của Bác sĩ Duy Ánh, xét nghiệm NIPT có độ chính xác >99% sẽ là lựa chọn giúp đánh giá kết quả chính xác hơn.

Xét nghiệm Double test có độ chính xác khoảng 70%
Xem bài viết chi tiết hơn về Xét nghiệm Double Test có chính xác không? 2 yếu tố ảnh hưởng
6. Xét nghiệm double test ở đâu uy tín?
Xét nghiệm sàng lọc trước sinh double test là xét nghiệm đại trà có mặt tại nhiều phòng khám, bệnh viện Để lựa chọn được địa chỉ ưng ý, mẹ cần quan tâm tới các tiêu chí như:
- Được cơ quan y tế cấp giấy phép
- Có máy móc, trang thiết bị hiện đại.
- Có đội ngũ y bác sĩ, kỹ thuật viên đủ kinh nghiệm và kỹ năng để thực hiện xét nghiệm.
Mẹ tham khảo 1 số đơn vị thực hiện double test uy tín như:
- Bệnh viện y Hà Nội
- Bệnh viện phụ sản Hà Nội
- Bệnh viện Medlatec
- Bệnh viện phụ sản trung ương
- Bệnh viện Hồng Ngọc
- Bệnh viện Vinmec
7. Lưu ý khi xét nghiệm sàng lọc trước sinh Double test
Quy trình xét nghiệm sàng lọc Double test đơn giản, kỹ thuật viên lấy khoảng 2 - 4 ml máu tĩnh mạch của mẹ sau đó đem đi xét nghiệm. Sau khoảng vài giờ đến vài ngày (tùy từng cơ sở), bác sĩ sẽ giải thích kết quả cho mẹ bầu. Để kết quả sàng lọc chính xác nhất, mẹ cần lưu ý:
- Thời điểm xét nghiệm: Nên xét nghiệm vào tuần thứ 11 - 13, vào buổi sáng và không cần nhịn ăn sáng.
- Cần thông báo với bác sĩ về loại thuốc đang dùng: Việc này giúp bác sĩ đánh giá kết quả chuẩn xác hơn.
- Cần mang theo sổ và kết quả khám lần trước: Việc này giúp bác sĩ theo dõi, đánh giá nguy cơ dị tật thai nhi chính xác hơn.
- Thông báo về tiền sử gia đình: Nếu gia đình bạn có người mắc bệnh di truyền hoặc vợ chồng được chẩn đoán có gen bệnh cần phải thông báo với bác sĩ để việc theo dõi, đánh giá kết quả được chính xác hơn.

Mẹ bầu cần thông báo với bác sĩ về tiền sử dị tật thai nhi, sức khỏe thai kỳ và các loại thuốc đang sử dụng
8. Thông số kết quả xét nghiệm Double test đọc thế nào?
Kết quả Double Test cho biết thai nhi có nguy cơ dị tật hay không, dựa trên ngưỡng an toàn:
- Đánh giá nguy cơ mắc bệnh Down: Ngưỡng an toàn với nguy cơ mắc hội chứng Down của thai nhi và tuổi của thai phụ là 1:250.
- Nguy cơ thấp mắc Down: Kết quả Double test cho mẫu số lớn hơn 250
- Nguy cơ cao mắc Down: Kết quả Double test cho mẫu số nhỏ hơn 250
- Đánh giá nguy cơ mắc bệnh Patau và Edward: Ngưỡng an toàn với nguy cơ mắc hội chứng này là 1:100:
- Nguy cơ thấp mắc bệnh Patau và Edward: Kết quả Double test cho mẫu số lớn hơn 100
- Nguy cơ cao mắc bệnh Patau và Edward: Kết quả Double test cho mẫu số nhỏ hơn 100
Sau khi có kết quả của từng loại dị tật, bác sĩ xét nghiệm sẽ kết luận về nguy cơ mắc dị tật và đưa ra lời khuyên cho mẹ nếu cần.

Phiếu sàng lọc kết quả Double test thông thường sẽ được giải thích nguy cơ gây dị tật và kết luận rõ ràng giúp mẹ dễ hiểu nhất
9. Giải đáp thắc mắc về xét nghiệm Double test
Phần dưới đây, chuyên gia GENTIS sẽ giải đáp một số câu hỏi về xét nghiệm sàng lọc trước sinh Double test, mẹ theo dõi để có thêm những kiến thức bổ ích nhất nhé!
9.1 Làm Double test rồi có cần làm Triple test không
Xét nghiệm Triple test là cần thiết phải thực hiện ở tuần 15 - 20 để phát hiện dị tật ống thần kinh hay không. Vì loại dị tật này không được sàng lọc ở Double test, mẹ nên thực hiện để kịp thời phát hiện.
Ngoài ra, với những mẹ có nguy cơ cao khi sàng lọc Double test, mẹ cần thực hiện thêm xét nghiệm này để giúp phát hiện các dị tật Down, Patau và Edward chính xác hơn.
9.2 Độ mờ da gáy bình thường có cần làm Double test
Độ mờ da gáy thường được kết hợp với Double test để xác định dị tật Down, việc này giúp tăng khả năng xác định nguy cơ dị tật thai nhi. Bên cạnh đó, Double test còn giúp sàng lọc thêm 2 loại nguy cơ khác là Edwards (Trisomy 18) và Patau (Trisomy 13). Vì thế, dù kết quả siêu âm đo độ mờ da gáy bình thường thì vẫn nên thực hiện Double test.

Độ mờ da gáy bình thường vẫn nên làm xét nghiệm sàng lọc trước sinh double test
Xét nghiệm sàng lọc trước sinh double test là cần thiết trong giai đoạn từ 11 - 13 tuần. Tuy nhiên, loại xét nghiệm này có độ chính xác chỉ khoảng 70%, nếu mẹ muốn kết quả sàng lọc chính xác hơn, mẹ có thể tham khảo phương pháp sàng lọc NIPT tại GENTIS chính xác >99%. GENTIS chúc mẹ và bé luôn mạnh khỏe, hạnh phúc.
[content_more] => [meta_title] => Tổng hợp kiến thức về xét nghiệm sàng lọc trước sinh Double Test [meta_description] => Xét nghiệm sàng lọc trước sinh Double test được thực hiện ở tuần thứ 11-13 của thai kỳ giúp phát hiện các dị tật như Down, hội chứng Edwards, Patau... [meta_keyword] => xét nghiệm sàng lọc trước sinh double test [thumbnail_alt] => xét nghiệm sàng lọc trước sinh double test [post_id] => 842 [category_id] => 15 ) [4] => stdClass Object ( [id] => 841 [id_crawler] => [category_product] => NULL [thumbnail] => tin-tuc/2022/t2/kham-sang-loc-truoc-sinh-co-can-nhin-an.jpg [album] => [url_video] => [is_status] => 1 [is_featured] => 0 [is_form] => 0 [displayed_time] => 0000-00-00 [program] => 0 [number] => 1 [viewed] => 0 [type] => [type_career] => [level] => [address] => [address_career] => [expiration_time] => 0000-00-00 [created_time] => 2022-02-28 02:17:53 [updated_time] => 2024-05-10 11:54:37 [files] => [salary] => [time] => [created_by] => 64 [is_table_content] => 1 [language_code] => vi [slug] => kham-sang-loc-truoc-sinh-co-can-nhin-an-khong [title] => Khám sàng lọc trước sinh có cần nhịn ăn không? Chuyên gia tư vấn [description] => Mẹ bầu lần đầu đi sàng lọc trước sinh nhưng không biết có cần nhịn ăn trước xét nghiệm không? Bài viết dưới đây sẽ giải đáp cho câu hỏi của mẹ, đồng thời tư vấn phương pháp và những chú ý trước khi đi sàng lọc trước sinh đảm bảo kết quả chính xác nhất. Mẹ bầu theo dõi nhé! [content] =>
Khám sàng lọc trước sinh có cần nhịn ăn không?
1. Có cần phải nhịn ăn khi khám sàng lọc trước sinh?
Theo chuyên gia, mẹ bầu không phải nhịn ăn trước khi khám sàng lọc trước sinh bằng các phương pháp double test, triple test và NIPT.
Cụ thể:
1.1. Double test
Xét nghiệm sàng lọc trước sinh double test là phương pháp đo nồng độ 2 hoạt chất trong máu mẹ gồm PAPP-A và free beta hCG. Từ đó dựa vào sự thay đổi nồng độ 2 chất này để tiên lượng khả năng thai mắc dị tật Down, Edward, Patau.
Phương pháp được thực hiện trong quý đầu mang thai (tuần 11 - 13 tuần 6 ngày) bằng cách lấy 2ml máu mẹ.
Trước khi xét nghiệm Double test thai phụ không cần nhịn ăn bởi PAPP-A và free beta hCG là hai loại protein do nhau thai tiết ra, không thay đổi theo chế độ ăn như các chỉ số Glucose máu, ure,...trong xét nghiệm sinh hóa máu thông thường.

Double test sàng lọc trước sinh bệnh Down ba cặp nhiễm sắc thể 21 với độ chính xác trên 80%
1.2. Triple test
Là phương pháp đo nồng độ 3 hoạt chất trong máu mẹ gồm AFP, free beta hCG và uE3. Từ đó dựa vào sự thay đổi nồng độ 3 chất này để tiên lượng khả năng thai mắc dị tật Down, Edward và dị dạng ống thần kinh.
Phương pháp được thực hiện trong quý 2 khi mang thai (tuần 15 - 20 tuần 6 ngày) bằng cách lấy 2ml máu mẹ. Được chỉ định khi mẹ bỏ lỡ sàng lọc trước sinh trong quý 1 hoặc sàng lọc trong quý 1 có kết quả thai nguy cơ cao dị tật.
Xét nghiệm Triple test khảo sát uE3 và free beta hCG là hai loại protein do nhau thai tiết ra kết hợp với AFP là protein do bào thai tiết ra. Nồng độ các chất này không phụ thuộc vào chế độ ăn, do đó thai phụ không cần nhịn ăn trước khi sàng lọc.

Triple test sàng lọc được các thai nhi có dị tật ống thần kinh nhờ đo nồng độ chất AFP
1.3. Sàng lọc trước sinh không xâm lấn NIPT Illumina (GenEva)
Đây là phương pháp mới ra đời năm 2010, bản chất là tách chiết các ADN tự do của thai nhi lưu hành trong máu mẹ từ đó định lượng nồng độ ADN, phân tích di truyền để khẳng định các đột biến lệch bội, mất đoạn NST gây dị tật bẩm sinh.
Phương pháp được thực hiện trong quý đầu mang thai (tuần 10 trở đi) bằng cách lấy 7 - 10ml máu mẹ.
cff ADN (ADN tự do của bào thai) xuất hiện từ tuần thứ 7, tồn tại suốt thời kỳ mang thai và mất đi sau sinh 2 giờ. Bởi cff ADN có nguồn gốc nhau thai, không thay đổi theo chế độ ăn của mẹ nên sản phụ trước khi làm NIPT Illumina không cần nhịn ăn.

Quy trình NIPT Illumina chỉ cần lấy máu đã sàng lọc được trên 12 dị tật phổ biến
2. Yếu tố ảnh hưởng đến kết quả khám sàng lọc trước sinh
Có rất nhiều yếu tố ảnh hưởng tới độ tin cậy của kết quả trong đó nổi bật có 3 yếu tố mẹ cần nắm được, đó là:
2.1. Cơ sở cung cấp dịch vụ sàng lọc
Theo một nghiên cứu [1], độ chính xác của kết quả khám sàng lọc trước sinh phụ thuộc vào: Chuyên gia tư vấn có kinh nghiệm, kỹ thuật xét nghiệm và độ tuổi của người mẹ.
→ Lời khuyên cho mẹ: Chọn địa chỉ khám uy tín, có nhiều phản hồi tích cực và được nhiều phụ huynh tin tưởng. Một đơn vị sàng lọc uy tín cần đảm bảo 3 tiêu chí:
- Công nghệ: Hiện đại, máy móc kỹ thuật có độ nhạy cao
- Chuyên gia: Có kinh nghiệm chuyên môn, có kỹ năng
- Cơ sở vật chất: Đạt tiêu chuẩn quốc tế

Cơ sở sàng lọc có nhiều chuyên gia kinh nghiệm là điểm tựa niềm tin cho mẹ
2.2. Yếu tố thuộc về mẹ
- Độ tuổi: Trước khi có các phương pháp sàng lọc trước sinh không xâm lấn, tuổi mẹ là tiêu chí đánh giá nguy cơ quan trọng quyết định sản phụ có cần được can thiệp xâm lấn (chọc ối, sinh thiết gai nhau) hay không. Với các biện pháp xâm lấn thực hiện trên sản phụ cao tuổi, nguy cơ biến chứng chảy máu, rò ối, nhiễm trùng có thể tăng cao.
- Bệnh lý hiện tại của mẹ: Trường hợp mẹ có tiền sử sẩy thai, HIV, bất đồng nhóm máu, rau tiền đạo, mắc bệnh ác tính sẽ có chống chỉ định với từng phương pháp sàng lọc khác nhau bởi tăng nguy cơ sẩy thai.

Tất cả phụ nữ mang thai cần được sàng lọc bệnh truyền nhiễm và xét nghiệm máu để tránh các biến chứng của sàng lọc trước sinh
2.3. Thời điểm sàng lọc trước sinh
Tùy từng cơ sở của mỗi phương pháp sàng lọc mà thời điểm sàng lọc có sự khác biệt. Mặt khác, thai nhi lớn lên từng ngày trong tử cung người mẹ, vào mỗi giai đoạn phát triển, thai lại có những dấu mốc nhận biết khác nhau. Do đó, mỗi phương pháp sàng lọc lại có giá trị riêng và không có biện pháp nào hoàn toàn bị loại bỏ hoàn toàn khỏi chương trình sàng lọc trước sinh.
Thời điểm “vàng” cho sàng lọc trước sinh là vào quý đầu thời kỳ mang thai, thường là vào tuần 10 - 13. Thời điểm này có thể phát hiện sớm các dị tật bẩm sinh nặng, giúp gia đình chuẩn bị tâm lý và đưa ra những quyết định dựa trên sự tư vấn của bác sĩ.

Thời điểm sàng lọc dị tật bẩm sinh tốt nhất là vào tam cá nguyệt đầu tiên của thai kỳ
3. 4 lưu ý cho mẹ bầu khám sàng lọc trước sinh lần đầu (tuần thứ 12)
- Trước khi làm xét nghiệm không nên sử dụng chất kích thích như đồ uống chứa cồn (rượu, bia), thuốc lá. Những chất này ảnh hưởng tới các chỉ số sinh tồn của mẹ cũng như tâm lý, sẽ khó khăn khi thực hiện các thủ thuật xâm lấn (chọc ối, sinh thiết gai nhau). Mẹ nên tránh khói thuốc lá, dùng đồ uống có cồn trước sàng lọc 1 tuần.
- Mẹ chuẩn bị tốt tâm lý thoải mái. Một tâm lý thoải mái sẽ giúp các thủ thuật diễn ra nhanh chóng, hạn chế ảnh hưởng tới mẹ và thai. Để tâm lý được thoải mái, trước sàng lọc mẹ cần ngủ sớm và ăn uống đầy đủ.
- Lựa chọn phương pháp sàng lọc an toàn, chính xác cho kết quả nhanh. Các phương pháp không xâm lấn, an toàn cao hiện nay được đưa vào sàng lọc thường quy bao gồm: Combine test (Double test và đo độ mờ da gáy), triple test, siêu âm, NIPT. Cho đến nay, NIPT Illumina là kỹ thuật sàng lọc trước sinh thực hiện được sớm nhất, tiết kiệm số lần sàng lọc và cho gia đình cơ hội đưa ra quyết định chấm dứt thai kỳ sớm, tránh ảnh hưởng sức khỏe thai phụ.
- Chọn phương pháp sàng lọc có độ chính xác cao, an toàn cho thai nhi. Phương pháp có độ chính xác cao nhất, sàng lọc được nhiều bệnh nhất nhưng hoàn toàn không ảnh hưởng tới thai hiện nay là NIPT Illumina. NIPT cho kết quả có độ chính xác >99% với các chẩn đoán âm và trên 85% với các chẩn đoán dương (có dị tật).

Lựa chọn phương pháp sàng lọc dị tật bẩm sinh cần có sự tư vấn của bác sĩ
NIPT Illumina là kỹ thuật sàng lọc trước sinh hàng đầu được các bác sĩ chuyên ngành Sản khoa bệnh viện tuyến trung ương khuyên mẹ thực hiện hiện nay.
Với những kỹ thuật mới, tiên tiết nhất trong lĩnh vực sàng lọc trước sinh, các phòng xét nghiệm tư hiện đang đi đầu về xu hướng. Một địa chỉ đảm bảo chất lượng mà cha mẹ có thể gửi gắm niềm tin cần có bề dày kinh nghiệm thể hiên qua số năm hoạt động, đội ngũ chuyên gia và máy móc.
Liên kết với các bệnh viện trung ương tại 2 thành phố lớn Hà Nội và Hồ Chí Minh, GENTIS là đơn vị tiên phong, cũng là đơn vị uy tín thực hiện khám sàng lọc trước sinh với 6 ưu điểm nổi bật:
- Công nghệ: Máy giải trình tự NextSeq 550 của hãng Illumina - Mỹ, 1 trong những máy giải trình tự gen hiện đại nhất hiện đại nhất ở Việt Nam hiện nay có độ chính xác cao và có thể phát hiện cả những dị tật mang tính chất di truyền
- Chuyên gia uy tín: PGS.BS Vũ Bá Quyết - Nguyên Giám đốc Bệnh viện Phụ sản Trung Ương.
- Trung tâm xét nghiệm đạt tiêu chuẩn quốc tế: Được cấp chứng chỉ ISO 15189:2012 (ISO 15189 là Tiêu chuẩn Yêu cầu về chất lượng và năng lực của phòng xét nghiệm Y tế)
- Kết quả chính xác >99%, độ nhạy và độ đặc hiệu cao phát hiện những bất thường cấu trúc NST.
- Sàng lọc được nhiều hội chứng di truyền gồm các đột biến lệch bội NST (Down, Edward, Patau) và đột biến mất đoạn nhiễm sắc thể ( Cri du chat, Di Geogre, Prader Willi,...)
- Hỗ trợ thu thập mẫu xét nghiệm tại nhà. QUy trình lấy mẫu tại nhà được thực hiện chuyên nghiệp, đúng kỹ thuật tương tự như tại mỗi cơ sỏ của GENTIS bởi các kỹ thuật viên dày dặn kinh nghiệm.

Đại tá Hà Quốc Khanh - Phó viện trưởng viện khoa học hình sự bộ công an, cố vấn chuyên môn của GENTIS nhận giấy chứng nhận phòng xét nghiệm đạt chuẩn quốc tế
Như vậy, trước bất kỳ thủ thuật, xét nghiệm sàng lọc trước sinh nào, việc nhịn ăn đều là không cần thiết. Mọi thông tin thắc mắc, cần tư vấn về sàng lọc trước sinh công nghệ mới NIPT Illumina (GenEva) xin quý khách hàng liên hệ với GENTIS qua hotline 0988002010 hoặc trực tiếp tới cơ sở tại Hà Nội (Tầng 3, Trung tâm thương mại V+, 505 Minh Khai, Vĩnh Tuy, Hai Bà Trưng, Hà Nội) và cơ sở thành phố Hồ Chí Minh (8/24 Nguyễn Đình Khơi, phường 4 Quận Tân Bình).
[content_more] => [meta_title] => Khám sàng lọc trước sinh có cần nhịn ăn không? Chuyên gia tư vấn [meta_description] => Mẹ bầu lần đầu đi sàng lọc trước sinh nhưng không biết có cần nhịn ăn trước xét nghiệm không? Bài viết dưới đây sẽ giải đáp cho câu hỏi của mẹ. [meta_keyword] => Khám sàng lọc trước sinh có cần nhịn ăn không [thumbnail_alt] => Khám sàng lọc trước sinh có cần nhịn ăn không [post_id] => 841 [category_id] => 15 ) [5] => stdClass Object ( [id] => 840 [id_crawler] => [category_product] => NULL [thumbnail] => tin-tuc/2022/t2/di-tat-lien-quan-den-gen-co-kha-nang-di-truyen.jpg [album] => [url_video] => [is_status] => 1 [is_featured] => 0 [is_form] => 0 [displayed_time] => 0000-00-00 [program] => 0 [number] => 1 [viewed] => 0 [type] => [type_career] => [level] => [address] => [address_career] => [expiration_time] => 0000-00-00 [created_time] => 2022-02-28 01:46:46 [updated_time] => 2022-05-09 13:42:19 [files] => [salary] => [time] => [created_by] => 64 [is_table_content] => 1 [language_code] => vi [slug] => di-tat-bam-sinh-co-di-truyen-khong [title] => Dị tật bẩm sinh có di truyền không? Cách ngăn ngừa từ sớm [description] => Dị tật bẩm sinh có di truyền không? Câu trả lời là có, tuy nhiên không phải 100% bố mẹ có Gen dị tật thì đều di truyền sang con. Vậy dị tật bẩm sinh do đâu? Làm thế nào để ngăn ngừa hiệu quả? Mẹ theo dõi tư vấn của chuyên gia GENTIS trong bài viết dưới đây! [content] =>1. Dị tật bẩm sinh có di truyền không?
Theo nghiên cứu của CDC [1], dị tật thai nhi do nhiều yếu tố khác nhau. Những yếu tố này bao gồm gen của bố mẹ và những tác động khác từ bên ngoài khi mẹ mang bầu như tuổi cao, sử dụng thuốc gây dị tật, mắc bệnh virus,...
Với các loại dị tật liên quan đến gen thì có khả năng di truyền từ bố mẹ sang con. Tuy nhiên không phải 100% bố mẹ mang gen dị tật, con sinh ra sẽ bị dị tật vì chúng còn phụ thuộc vào từng loại gen và từng cá thể riêng biệt.
Nếu chẳng may người nhà mình mắc một số bệnh về dị tật, hoặc phát hiện ra bố mẹ có gen dị tật bẩm sinh thì mẹ cũng đừng lo lắng quá. Thay vào đó mẹ cần thăm khám và sàng lọc đúng định kỳ để bác sĩ chẩn đoán dị tật chính xác nhất.

Các dị tật liên quan tới Gen có khả năng di truyền
Hầu hết các loại dị tật đều có nguy cơ di truyền, trong đó một số bệnh liên quan đến máu và hệ thống là điển hình nhất, ví dụ: Thalassemia, dị tật tim bẩm sinh, dị tật điếc bẩm sinh,...
Mẹ bầu dễ mang thai nhi bị dị tật bẩm sinh do di truyền khi:
- Mẹ trên 35 tuổi
- Con cái, hoặc anh chị em trong nhà bị dị tật
- Mẹ đã từng mang thai bị dị tật
2. Phải làm sao khi mẹ bầu có nguy cơ di truyền dị tật cho con?
Với mẹ bầu từng mang thai bị dị tật, có tiền sử sảy thai hoặc người nhà bị dị tật cần chú ý để ngăn ngừa dị tật bẩm sinh bằng cách:
1 - Lập kế hoạch mang thai
- Kiểm tra sức khỏe trước khi mang thai: Cả bố và mẹ cần phải kiểm tra, sàng lọc xem có bất thường về gen hoặc có nguy cơ mắc bệnh di truyền gì không? Nếu có bác sĩ sẽ đưa ra hướng dẫn phù hợp nhất để tránh sinh con bị dị tật.
- Tiêm phòng: Với mẹ có nguy cơ mang thai bị dị tật, mẹ cần chủ động tiêm phòng các loại vacxin như cúm mùa, rubella, sởi, quai bị,.... để ngăn ngừa virus xâm nhập trong thai kỳ, tránh dị tật thai nhi.
- Bổ sung acid folic: Bổ sung acid folic trước mang thai giúp ngăn ngừa các dị tật liên quan tới ống thần kinh và tủy xương.

Mẹ chủ động bổ sung acid folic để ngăn ngừa dị tật thai nhi
2 - Theo dõi dị tật thai nhi định kỳ
Mẹ cần thăm khám đầy đủ ở các tuần thứ 10 - 14, 16 - 20, 30 - 32. Đồng thời mẹ cần lựa chọn phương pháp sàng lọc có độ chính xác cao, phát hiện dị tật từ sớm để có phương án xử lý kịp thời, đảm bảo an toàn cho mẹ nhất.
3 - Chăm sóc sức khỏe khoa học
- Chế độ ăn uống: Mẹ cần ăn uống đầy đủ các chất để thai nhi khỏe mạnh, phát triển các bộ phận trên cơ thể ngăn ngừa dị tật. Đồng thời mẹ lựa chọn nguồn thực phẩm có nguồn gốc xuất xứ rõ ràng, tránh bị phun thuốc trừ sâu, chất bảo quản gây độc cho tế bào thai gây dị tật.
- Tập luyện thể dục: Việc này giúp tăng cường đề kháng, ngăn ngừa các bệnh do vi khuẩn, virus gây dị tật thai nhi
- Không tùy ý sử dụng thuốc bừa bãi trong thai kỳ: Vì rất nhiều thuốc làm tăng nguy cơ dị tật thai nhi, thậm chí gây sảy thai.
3. Giải đáp thắc mắc về dị tật bẩm sinh
3.1. Thai nhi bị dị tật phải làm sao?
Nếu chẳng may mẹ đi khám sàng lọc và phát hiện thai nhi bị dị tật, lúc này mẹ cần bình tĩnh, chăm sóc sức khỏe tốt để tránh ảnh hưởng tới thai nhi. Nếu kết quả sàng lọc dựa trên Double test hoặc Triple test, mẹ chưa cần vội hoang mang, vì độ chính xác mới chỉ 75%, vẫn có thể có sai sót. Do đó, mẹ cần tới các đơn vị uy tín để thực hiện thêm các sàng lọc như NIPT hoặc chọc ối,... để được bác sĩ chẩn đoán chính xác nhất. Mẹ tham khảo thêm phương pháp sàng lọc dị tật thai nhi GENEVA thực hiện trên công nghệ Illumina - Mỹ có độ chính xác >99%.

Nếu thai nhi bị dị tật, mẹ cần tham khảo ý kiến bác sĩ để có phương án xử lý kịp thời
Với những thai phụ đã được chẩn đoán dị tật thai nhi, mẹ cần cụ thể xem loại dị tật thai nhi có thể chữa được không, mong muốn của gia đình để có giải pháp phù hợp nhất. Thông thường, với các dị tật như hở hàm ếch, sứt môi,... có thể đơn giản chữa trị. Còn các dị tật hệ thống như thiếu hụt chi, hở van tim, khuyết tật các bộ phận bên trong cơ thể,... sẽ khó chữa và cần nhiều chi phí, kết quả điều trị không cao.
3.2. Những loại thuốc gây dị tật thai nhi mẹ bầu nên tránh
Theo lời khuyên của chuyên gia, mẹ bầu không nên tùy ý sử dụng thuốc trong thời kỳ mang thai vì tiềm ẩn nguy cơ gây dị tật, ảnh hưởng trực tiếp tới sức khỏe mẹ bầu và thai nhi. Tốt nhất, mẹ nên tham khảo ý kiến bác sĩ, dược sĩ về các loại thuốc và cách sử dụng nhé!

Mẹ bầu không tự ý sử dụng thuốc khi chưa có ý kiến của bác sĩ
Mẹ thêm khảo thêm: Điểm mặt 15+ nhóm thuốc gây dị tật thai nhi cần tránh
Đọc đến đây, mẹ đã tìm được câu trả lời cho câu hỏi dị tật bẩm sinh có di truyền không? Mặc dù có nguy cơ di truyền tuy nhiên không phải 100%. Mẹ lưu ý, khi nghi ngờ bản thân hoặc chồng có thể mang GEN bệnh di truyền, mẹ cần lên kế hoạch để thăm khám bác sĩ, được tư vấn và lựa chọn cách mang thai, sinh con an toàn nhất nhé!
1. Dị tật thai nhi có chữa được không?
Dị tật thai nhi có chữa được không phụ thuộc loại dị tật, sức khỏe của thai nhi và kỹ thuật y khoa.
Cụ thể như sau:
- Tại Việt Nam: Theo chuyên gia, các dị tật có thể chữa khỏi như: Dị tật như sứt môi, hở hàm ếch. Bác sĩ sẽ can thiệp và chữa sau khi bé chào đời.
- Ở các nước phát triển: Có thể trị được thêm các vấn đề như:
- Thoát vị hoành bẩm sinh: Tình trạng này, trong đó một lỗ trên cơ hoành cho phép chất trong bụng đi vào ngực và hạn chế sự phát triển của phổi, có thể được giúp đỡ đáng kể trong tử cung thông qua phương pháp tắc nội khí quản qua nội soi, một phẫu thuật giúp cải thiện chức năng phổi và tăng đáng kể tỷ lệ sống sót.
- Tắc nghẽn đường tiết niệu dưới: Điều này xảy ra khi dòng chảy của nước tiểu bị chặn lại không thể thoát ra khỏi cơ thể của thai nhi, dẫn đến tổn thương thận vĩnh viễn. Giảm tắc nghẽn này trước khi sinh sẽ bảo vệ thận.
Các dị tật không thể chữa được: Dị tật bẩm sinh về gen, mang tính hệ thống như dị tật tim bẩm sinh, dị tật thần kinh, bất thường số lượng nhiễm sắc thể là không thể chữa khỏi. Đồng thời, các dị tật này có chi phí điều trị phức tạp cao, tốn kém và có nguy cơ tử vong cao.

Các dị tật như sứt môi, hở hàm ếch có thể chữa sau khi bé chào đời từ 1 - 3 tuổi
2. Thai nhi bị dị tật nên làm gì?
Nếu chẳng may thai nhi bị dị tật, mẹ cần phải theo dõi cẩn thận theo lời khuyên của bác sĩ.
2.1 Theo dõi dị tật thai nhi theo lời khuyên bác sĩ
Các loại xét nghiệm dị tật thai nhi như Double test hoặc Triple test chỉ có ý nghĩa sàng lọc, không có ý nghĩa chẩn đoán. Vì vậy, nếu mẹ mới chỉ thực hiện các xét nghiệm này thuộc nhóm nguy cơ cao không có nghĩa 100% thai nhi bị dị tật. Lúc này mẹ cần tuân thủ hướng dẫn của bác sĩ, thực hiện thêm các xét nghiệm sàng lọc dị tật thai nhi như NIPT để cho kết quả chính xác >99%.
Khi lựa chọn đơn vị sàng lọc dị tật, mẹ cần chọn đơn vị uy tín, được cấp phép bởi cơ quan y tế, đánh giá cao của chuyên gia và người tiêu dùng. Mẹ có thể tham khảo phương pháp sàng lọc dị tật thai nhi NIPT của GENTIS có độ chính xác >99%. Đây là địa chỉ được PGS. Ts Vũ Bá Quyết cùng nhiều chuyên gia đầu ngành đánh giá cao và nhiều mẹ Việt nổi tiếng lựa chọn.

GENEVA thực hiện trên công nghệ Illumina - Mỹ chính xác >99% đang được nhiều mẹ Việt lựa chọn để theo dõi dị tật thai nhi
2.2 Chấm dứt thai kỳ theo chỉ định của bác sĩ
Các dị tật về gen và mang tính hệ thống như khuyết tật, dị tật ống thần kinh, dị tật tim, khuyết tật lồng ngực và khớp, điếc, mù, chậm phát triển trí tuệ,... ảnh hưởng lớn tới sức khỏe và tương lai của trẻ sau này. Với các dị tật này, mẹ sẽ được khuyên chấm dứt thai kỳ càng sớm, càng tốt tránh để thai to khó xử lý và tốn kém, ảnh hưởng tới sức khỏe của mẹ. Lúc này mẹ bầu và gia đình nên nghe lời khuyên của bác sĩ, phụ thuộc vào mong muốn và sức khỏe của thai nhi để có được lựa chọn phù hợp nhất.
Nếu gia đình có mong muốn chấm dứt thai kỳ, mẹ bầu cần chọn địa chỉ uy tín để thực hiện để đảm bảo an toàn nhất. Vì chỉ định y khoa chấm dứt thai kỳ rất nguy hiểm, cần phải thận trọng để không ảnh hưởng đến sức khỏe mẹ bầu và khả năng sinh sản sau này.
3. Hướng dẫn phòng chống và theo dõi dị tật thai nhi
Theo thống kê, hàng năm có tới khoảng 3% trẻ sơ sinh bị dị tật thai nhi chào đời. Nguyên nhân chủ yếu do mẹ chưa chủ động phòng chống và theo dõi dị tật lúc mang thai. Vậy làm thế nào để sinh con khỏe mạnh, hạn chế dị tật thai nhi nhất? Mẹ theo dõi ngay tư vấn của chuyên gia ở phần tiếp theo.
3.1 Sàng lọc dị tật thai nhi tuần thứ bao nhiêu?
Theo dõi và đi thăm khám dị tật thai nhi đúng thời điểm là chìa khóa vàng để mẹ kịp thời phát hiện bé yêu có khỏe mạnh không? Vì vậy mẹ đừng bỏ qua 3 thời điểm sàng lọc dị tật thai nhi đang được chuyên gia khuyến cáo đó là:
- Khoảng từ 10 tuần: Thực hiện sàng lọc NIPT để phát hiện dị tật thai nhi như: Hội chứng Down, Hội chứng Edwards, Hội chứng Patau, Hội chứng Turner, Hội chứng Klinefelter, Thể tam nhiễm XXX, Hội chứng Jacobs. Ngoài ra sàng lọc này còn phát hiện các đột biến vi mất đoạn: Mất đoạn 22q11 (DiGeorge), Mất đoạn 15q11 (Angelman/Prader - Willi), Mất đoạn 1p36, Wolf - Hirschhorn, Cri-du-cha và bất thường số lượng tất cả các NST còn lại
- Tuần 12 - 14: Sàng lọc Double test giúp phát hiện các hội chứng Trisomy 13 (thừa NST 13). Sàng lọc này kết hợp với siêu âm độ mờ da gáy còn phát hiện nguy cơ bị Down, dị tật chân tay, tim mạch, sứt môi, hở hàm... chính xác tới 90%.
- Tuần 18 - 20: Sàng lọc Triple test giúp chẩn đoán thêm các dị tật thai nhi khác như ống thần kinh.

Mẹ nên sàng lọc thai nhi từ tuần thứ 10, 12 -14 và 20 - 24 tuần tuổi
3.2. Phương pháp sàng lọc dị tật thai nhi nào an toàn, chính xác nhất?
Các phương pháp sàng lọc dị tật thai nhi như:
- Double test: Thực hiện ở tuần thứ 11 đến 13 của thai kỳ, độ chính xác khoảng 75%, chỉ có ý nghĩa sàng lọc, không có ý nghĩa chẩn đoán.
- Triple test: Thực hiện ở tuần thứ 21 - 24 của thai kỳ, độ chính xác khoảng 75%, chỉ có ý nghĩa sàng lọc, không có ý nghĩa chẩn đoán.
- NIPT: Có thể thực hiện từ tuần thứ 10 của thai kỳ, độ chính xác >99% và được dùng để chẩn đoán các dị tật thai nhi.
Hiện nay, NIPT là phương pháp sàng lọc dị tật thai nhi được chuyên gia đánh giá cao nhất về độ chính xác vì nó xét nghiệm trực tiếp ADN của thai. Tại GENTIS mẹ bầu sẽ được thăm khám tư vấn bởi đội ngũ chuyên gia nhiều năm kinh nghiệm. Đây là địa chỉ sàng lọc thai nhi uy tín mẹ bầu chớ bỏ qua nhé!

Xét nghiệm dị tật thai nhi tại GENTIS giúp mẹ sớm phát hiện dị tật bẩm sinh chính xác >99%
3.3. Những loại thuốc gây dị tật thai nhi mẹ bầu cần tránh
Theo ý kiến của chuyên gia y tế, mẹ bầu không nên tự ý sử dụng bất cứ loại thuốc nào khi chưa có ý kiến của bác sĩ. Vì sử dụng thuốc không phù hợp có thể gây dị tật thai nhi, ảnh hưởng trực tiếp tới tính mạng của cả mẹ và bé.
Một số loại thuốc có nguy cơ gây dị tật thai nhi cao như: Thuốc chống trầm cảm, thuốc kháng sinh, thuốc an thần, thuốc tim mạch, thuốc hạ đường huyết.
Để tìm hiểu chi tiết về thuốc gây dị tật thai nhi, mẹ tham khảo bài viết này: Những thuốc gây dị tật thai nhi cần tránh

Mẹ bầu không tùy ý sử dụng thuốc khi chưa có hướng dẫn của dược sĩ hoặc bác sĩ vì có thể gây dị tật thai nhi bẩm sinh không chữa được
Như vậy, dị tật thai nhi có chữa được không phụ thuộc vào loại dị tật và cơ sở y tế. Nếu chẳng may thai nhi bị dị tật, mẹ hãy bình tĩnh và tham khảo ý kiến bác sĩ để được thăm khám kỹ lưỡng và có phương án phù hợp. Để đảm bảo an toàn cho thai nhi, mẹ cần theo dõi và sàng lọc thai nhi định kỳ, để kịp thời phát hiện dị tật. GENTIS chúc mẹ bầu khỏe mạnh, mẹ tròn con vuông nhé!
[content_more] => [meta_title] => Dị tật thai nhi có chữa được không: Tư vấn từ chuyên gia [meta_description] => Dị tật thai nhi có chữa được không phụ thuộc vào loại dị tật, sự phát triển của nền y học. Để tìm hiểu kỹ hơn về vấn đề này, mẹ tham khảo tư vấn của chuyên gia GENTIS trong bài viết sau nhé! [meta_keyword] => dị tật thai nhi có chữa được không [thumbnail_alt] => dị tật thai nhi có chữa được không [post_id] => 839 [category_id] => 15 ) [7] => stdClass Object ( [id] => 838 [id_crawler] => [category_product] => NULL [thumbnail] => tin-tuc/2022/t2/di-tat-thai-nhi-lam-sao-de-ngan-ngua.jpg [album] => [url_video] => [is_status] => 1 [is_featured] => 0 [is_form] => 0 [displayed_time] => 0000-00-00 [program] => 0 [number] => 1 [viewed] => 0 [type] => [type_career] => [level] => [address] => [address_career] => [expiration_time] => 0000-00-00 [created_time] => 2022-02-28 00:51:57 [updated_time] => 2022-05-09 13:29:36 [files] => [salary] => [time] => [created_by] => 64 [is_table_content] => 1 [language_code] => vi [slug] => ngan-ngua-di-tat-thai-nhi [title] => 9 bí quyết ngăn ngừa dị tật thai nhi mẹ bầu cần biết [description] => Theo thống kê thực tế ngành y tế, Việt Nam mỗi năm có khoảng 1,5 - 2% trẻ em sinh ra bị mắc dị tật bẩm sinh. Vậy dị tật thai nhi làm sao để ngăn ngừa, phòng tránh? - Đây chính là nỗi băn khoăn chung của tất cả mẹ bầu. Bài biết dưới đây sẽ chia sẻ cho mẹ 9 bí quyết ngăn ngừa dị tật thai nhi dễ thực hiện và hiệu quả nhất. Mẹ tham khảo nhé! [content] =>
Việt Nam mỗi năm có khoảng 1,5 - 2% trẻ em sinh ra bị mắc các dị tật bẩm sinh. Bài viết dưới đây mách mẹ 9 bí quyết ngăn ngừa dị tật thai nhi
1. Dị tật thai nhi có thể ngăn ngừa được không?
Các chuyên gia của GENTIS khẳng định với mẹ là: Dị tật bẩm sinh không thể ngăn ngừa 100%, không có một loại thuốc cụ thể hay thực phẩm nào có thể ngăn ngừa hoàn toàn vấn đề này. Tuy nhiên, mẹ bầu có thể yên tâm rằng dị tật thai nhi có thể phòng ngừa nếu mẹ bầu thực hiện đúng những lời khuyên của bác sĩ và khám thai định kỳ theo hướng dẫn.
2. 4 cách ngăn ngừa dị tật thai nhi trước thai kỳ
Trẻ có thể mắc dị tật bẩm sinh ngay từ trong bụng mẹ, từ những dị tật nhỏ: sứt môi, hở hàm ếch… đến dị tật lớn, chẳng hạn như: dị tật thai nhi đầu nhỏ, khuyết tật ống thần kinh, hội chứng Down… Dưới đây là 4 cách ngăn ngừa dị tật thai nhi trước thai kỳ, mẹ tham khảo:
2.1. Xét nghiệm di truyền
Nếu mẹ có gen bất thường nhưng không mắc bệnh thì mẹ được coi là mang gen bệnh. Xét nghiệm di truyền giúp sàng lọc gen mang bệnh ở mẹ và cho biết khả năng mẹ truyền gen này cho con.
Để kiểm tra mẹ có mang bệnh di truyền hay không, bác sĩ tiến hành lấy mẫu nước bọt hoặc máu của mẹ. Sau đó, mẫu được chuyển đến phòng thí nghiệm để kiểm tra.

Mẹ được tiến hành lấy mẫu máu để xét nghiệm di truyền trước khi mang thai
2.2. Khám tiền sản trước khi mang thai
Trước khi mang thai, mẹ nên chủ động khám tiền sản để đảm bảo mẹ khỏe mạnh, không mắc các bệnh lý nghiêm trọng và sẵn sàng cho kế hoạch có em bé. Trường hợp mẹ mắc các bệnh lý có thể gây tác động xấu đến sức khỏe bé, mẹ cần trao đổi với bác sĩ để có kế hoạch điều trị phù hợp, đảm bảo em bé sinh ra có sức khỏe tốt.
Chất lượng của địa điểm khám tiền sản cũng rất quan trọng. Mẹ nên chọn những nơi có trang thiết bị y tế tốt, đội ngũ bác sĩ dày dặn chuyên môn.
2.3. Uống bổ sung acid folic sớm
Khi có ý định mang thai, mẹ cần bổ sung acid folic sớm ít nhất 3 tháng trước khi mang thai. Vì Axit folic là một loại vitamin B cần thiết để mọi tế bào trong cơ thể thai nhi tăng trưởng và phát triển bình thường. Đội ngũ chuyên gia của GENTIS khuyến khích chế độ ăn thường ngày của mẹ cần đáp ứng đủ 400mcg axit folic.

Axit folic là một loại vitamin B cần thiết để mọi tế bào trong cơ thể thai nhi tăng trưởng và phát triển bình thường
2.4. Tiêm phòng đầy đủ trước khi mang thai
Tiêm phòng trước khi mang thai là hết sức cần thiết để bảo vệ sức khỏe cho cả mẹ bầu và thai nhi. Cụ thể là:
- Tiêm phòng cúm: mẹ bị cúm khi đang mang thai làm tăng nguy cơ sinh non. Trẻ sinh non có thể gặp nhiều vấn đề về sức khỏe và phải nằm viện lâu hơn với trẻ sinh đủ tháng.
- Tiêm phòng vắc xin sởi - quai bị - rubella, các bệnh này có thể gây ra các vấn đề nghiêm trọng trong thai kỳ như sẩy thai, thai chết lưu, sinh non, thai mắc dị tật bẩm sinh (dị tật tim, các vấn đề về thị lực và thính giác)
- Tiêm phòng bệnh thủy đậu: mẹ mắc bệnh thủy đậu khi đang mang bầu có thể gây ra các khiếm khuyết về hình dạng hoặc chức năng của một hoặc nhiều bộ phận trên cơ thể em bé. Lưu ý: Sau 1 tháng tiêm vắc xin phòng thủy đậu mẹ mới nên có kế hoạch mang thai.
- Một số loại khác: viêm gan A, viêm gan B…

Mẹ được tiêm phòng đúng loại, đúng thời điểm sẽ giúp mẹ khỏe mạnh, bé sinh ra không bị ốm nặng hoặc gặp các vấn đề sức khỏe suốt đời
3. 5 cách giảm rủi ro dị tật thai nhi trong thai kỳ
Để phòng tránh dị tật bẩm sinh cho thai nhi trong thai kỳ, đảm bảo bé sinh ra khỏe mạnh, mẹ cần ghi nhớ những lưu ý quan trọng sau:
3.1. Chỉ dùng thuốc khi có chỉ định bác sĩ
Trước khi dùng bất kỳ loại thuốc nào (kể cả thuốc không kê đơn) hoặc thực phẩm chức năng (bao gồm cả dược liệu), phụ nữ mang thai nên tham khảo ý kiến bác sĩ.
Sau đây là một vài ví dụ về những thuốc có thể gây ra dị tật thai nhi:
- Isotretinoin là một dạng dẫn xuất của vitamin A được sử dụng để điều trị mụn trứng cá gây ra những bất thường về tim, thận, ống thần kinh cho thai nhi. Mẹ được khuyến cáo nên đợi ít nhất 3 đến 4 tuần sau khi ngừng thuốc rồi mới nên mang thai.
- Thuốc chống trầm cảm: fluoxetine, paroxetine… Nghiên cứu [1] chỉ ra rằng mẹ bầu dùng thuốc chống trầm cảm có thể gây nứt đốt sống, dị tật tim và các dị tật bẩm sinh khác cho bào thai.
3.2. Tránh sử dụng các yếu tố gây hại đến sức khỏe thai nhi
Mẹ cần tránh sử dụng các yếu tố gây hại đến sức khỏe thai nhi như:
- Rượu: mẹ uống rượu khi mang thai có thể gây sẩy thai, thai chết lưu và một loạt các khuyết tật về thể chất và trí tuệ suốt đời cho trẻ.
- Thuốc lá: mẹ bầu hút thuốc lá có thể dẫn đến hậu quả sinh non, dị tật bẩm sinh (sứt môi hoặc hở hàm ếch). Các vấn đề này vẫn có thể xảy ra nếu môi trường xung quanh mẹ có nhiều khói thuốc lá.

Môi trường xung quanh mẹ có nhiều khói thuốc lá có thể dẫn đến hậu quả sinh non, dị tật bẩm sinh (sứt môi hoặc hở hàm ếch).
3.3. Chế độ sinh hoạt khoa học
Để phòng dị tật thai nhi bẩm sinh, mẹ nên thực hiện chế độ sinh hoạt khoa học bằng cách kết hợp chế độ ăn uống đầy đủ dưỡng chất và vận động hợp lý.
- Chế độ ăn uống: bên cạnh chế độ dinh dưỡng đủ chất mẹ bầu cần kiểm soát tốt lượng đường trong máu để giảm thiểu nguy cơ mắc tiểu đường thai kỳ. Điều này giúp kiểm soát những biến chứng thai kỳ nghiêm trọng, giảm rủi ro thai nhi mắc dị tật. Do vậy, mẹ hãy chú trọng ăn nhiều thực phẩm giàu chất xơ như: rau xanh, hoa quả, hạt chia…
- Vận động vừa sức trong suốt quá trình mang bầu giúp mẹ duy trì được cân nặng, đẩy lùi nguy cơ béo phì, duy trì sức khỏe tốt cho cả mẹ và bé. Bởi mẹ bị béo phì là yếu tố nguy cơ gây ra những khiếm khuyết thai nhi bẩm sinh. Mẹ nên chọn các bài tập yoga nhẹ nhàng hoặc đi bộ 20 - 30 phút mỗi ngày.

Mẹ dành ra 20 - 30 mỗi ngày để đi bộ nhẹ nhàng se đẩy lùi nguy cơ béo phì.
4. Cách phát hiện sớm dị tật thai nhi mẹ bầu cần biết
Dù mẹ áp dụng các cách phòng tránh nêu trên thì vẫn có nguy cơ thai nhi mắc các dị tật. Để có giải pháp sớm, giảm thiểu các tình huống xấu xảy ra thì mẹ nên:
4.1. Khám thai định kỳ
Khám thai định kỳ là cách theo dõi thường xuyên những thay đổi trong quá trình lớn lên của thai nhi. Qua đó, bác sĩ xác định các vấn đề sức khỏe bất thường của em bé có thể xảy ra trong thai kỳ hoặc sau khi sinh.

Khám thai định kỳ giúp theo dõi thường xuyên những thay đổi trong quá trình lớn lên của thai nhi giúp xác định các vấn đề sức khỏe bất thường của em bé có thể xảy ra trong thai kỳ
4.2. Thực hiện sàng lọc trước sinh
Mẹ thực hiện sàng lọc trước sinh sẽ giúp nhận biết được tình trạng sức khỏe của thai nhi trong bụng nhằm có hướng chăm sóc thai nhi phù hợp nhất.
Hiện nay có nhiều xét nghiệm sàng lọc: siêu âm thai, đo nồng độ AFP trong máu mẹ… Trong đó, phương pháp sàng lọc trước sinh không xâm lấn NIPT illumina là phương pháp sàng lọc được tin dùng nhất vì an toàn (không xâm lấn) và chính xác >99%.

Trung tâm xét nghiệm quốc tế GENTIS là đơn vị uy tín cung cấp các dịch vụ xét nghiệm sàng lọc dị tật trước sinh
Trung tâm xét nghiệm quốc tế GENTIS là đơn vị đầu tiên tại Việt Nam được nhận chứng nhận từ Illumina - Tổ chức giải mã gen lớn nhất thế giới - là địa chỉ tin cậy hàng đầu của mẹ bầu. Những ưu điểm của xét nghiệm NIPT Illumina (GenEva) tại GENTIS có thể kể đến như:
- Công nghệ hiện đại, đạt tiêu chuẩn quốc tế: xét nghiệm NIPT Illumina (GenEva) được thực hiện tại phòng xét nghiệm quốc tế GENTIS đạt chứng chỉ ISO 15189:2012. Điều này giúp xét nghiệm NIPT tại GENTIS phát hiện chính xác >99% hội chứng Down và các bất thường nhiễm sắc thể khác. Do vậy, mẹ hoàn toàn có thể yên tâm về kết quả mà không cần làm thêm các xét nghiệm có rủi ro như: chọc ối, sinh thiết gai nhau…
- An toàn: khác với kỹ thuật chọc ối có xâm lấn, khi thực hiện xét nghiệm NIPT tại GENTIS, bác sĩ chỉ lấy 7ml máu tĩnh mạch của thai phụ nên khắc phục được rủi ro nhiễm trùng cho mẹ bầu.
- Thời gian trả kết quả nhanh: nhờ áp dụng công nghệ hiện đại nên kết quả xét nghiệm NIPT tại GENTIS được trả về sớm nhất là sau 5 ngày thực hiện xét nghiệm. Nhờ đó, mẹ không mất nhiều thời gian chờ đợi kết quả trong lo lắng.
- Đội ngũ chuyên gia lâu năm giàu kinh nghiệm: đến với trung tâm xét nghiệm quốc tế GENTIS, mẹ sẽ được thăm khám bởi đội ngũ chuyên gia hàng đầu trong lĩnh vực di truyền, các bác sĩ sản khoa uy tín trên cả nước.
Hy vọng bài viết trên đây đã giúp mẹ bầu biết dị tật thai nhi làm sao để phòng ngừa! Mọi thắc mắc mẹ liên hệ qua số hotline của GENTIS 0988 002 010 để được chuyên gia giải tư vấn tận tình.
2 loại dị tật thai nhi mọc đuôi & Cách phát hiện sớm, chính xác
Hướng dẫn chi tiết A - Z về kết quả sàng lọc trước sinh double test
Xét nghiệm Double Test có chính xác không? 2 yếu tố ảnh hưởng
Tổng hợp kiến thức về xét nghiệm sàng lọc trước sinh Double Test
Khám sàng lọc trước sinh có cần nhịn ăn không? Chuyên gia tư vấn
Dị tật bẩm sinh có di truyền không? Cách ngăn ngừa từ sớm
Dị tật thai nhi có chữa được không: Tư vấn từ chuyên gia
9 bí quyết ngăn ngừa dị tật thai nhi mẹ bầu cần biết
Quý khách vui lòng điền thông tin bên dưới để được hỗ trợ,
tư vấn một cách tốt nhất!
Quý khách vui lòng điền thông tin bên dưới để được hỗ trợ,
tư vấn một cách tốt nhất!